Qu'est-ce que la focalisation hyperéchogène. Focalisation hyperéchogène dans le ventricule gauche du cœur fœtal: qu'est-ce que c'est et à quel point est-ce dangereux. Méthodes d'examen supplémentaires
Lors de la deuxième échographie programmée, un foyer hyperéchogène dans le ventricule gauche du cœur fœtal est souvent détecté. Cette inclusion est un petit point - un accord supplémentaire, qui ne cause aucun dommage à l'enfant, mais à condition que la présence de pathologies chromosomiques soit exclue.
Description du diagnostic
Au lieu de localisation du point, un sceau du tissu cardiaque est trouvé, il peut être causé par:
Une étude prospective de Huang et al., qui a évalué 118 fœtus, a abouti à une prévalence de la trisomie 21 de 0,35 %, avec un nombre significativement plus élevé de fœtus atteints chez les femmes enceintes qui étaient positifs au dépistage combiné au premier trimestre, en les comparant à ceux dont les résultats dans ces études étaient normaux.
Bradley et al ont conclu en évaluant 875 fœtus qu'un foyer échogène isolé semble être une variante bénigne plutôt qu'un risque accru d'aneuploïdie fœtale. Cela a conduit à une conclusion similaire à celle énoncée dans le paragraphe précédent. Un foyer d'écho intracardiaque isolé est caractéristique commune observé au deuxième trimestre de la grossesse, et est un motif fréquent de recours à la consultation d'échocardiographie fœtale pour rejeter les anomalies structurelles qui surchargent inutilement ces services, les couples et leurs proches ajoutent à l'anxiété engendrée.
- gisements de sel;
- la présence d'une pathologie dans l'ensemble chromosomique;
- la présence d'un accord supplémentaire, qui n'affecte pas le travail complet du cœur.
Si la cause qui a provoqué l'apparition d'un point blanc dans la cavité du cœur est un grand nombre de sels, puis au troisième trimestre, il disparaît et n'entraîne aucune conséquence pour le fœtus. Il en va de même pour la corde, elle peut provoquer des souffles cardiaques jusqu'à un certain âge (passent généralement en 2-3 ans), ou disparaissent avant la naissance. Dans tous les cas, s'il est présent, il est nécessaire d'examiner régulièrement l'enfant avec un cardiologue.
Sa présence est associée à un risque accru d'infection fœtale causée par le syndrome de Down et d'autres aneuploïdes. À cet égard, nous partageons l'avis de plusieurs auteurs, confirmant que la présence d'un foyer échogène isolé chez les femmes enceintes de moins de 35 ans avec des marqueurs biochimiques normaux n'augmente pas le risque d'infection du fœtus avec une anomalie chromosomique.
Que faire lorsqu'un FEM est identifié
Institut national du travail et d'immunologie. . Congénital défaut 4-5% Toute anomalie morphologique, structurelle, fonctionnelle ou moléculaire présente à la naissance. Responsable de 30% de la mortalité périnatale dans les pays développés. Morbidité à la naissance en %.
Le danger n'est qu'un diagnostic trouvé en association avec des troubles chromosomiques. Dans ce cas, le compactage du myocarde est un danger pour la vie de l'enfant.
foyer hyperéchogène dans le ventricule gauche du cœur fœtal peut indiquer la présence du syndrome de Down, si des marqueurs chromosomiques pathologiques ont été détectés chez une femme enceinte lors d'un test sanguin.
Que faire en cas de pathologie ?
Maladies monogéniques héréditaires. Dépistage petit format Dépistage petit format Dépistage chromosomique Dépistage dépistage chromosomique. Morphologie écomorphologique. Norme de dépistage par niveaux. Incidence des malformations Risque malformatif faible 2,6 % Risque malformatif élevé 7,4 %.
Dépistage des malformations pour toutes les femmes enceintes. Recommande. Réalisation d'une éco-compétence de 20 semaines. Doté de moyens techniques. Assurez la qualité de la numérisation. Indiquez clairement que le taux de détection des défauts est de 70 %.
Combien de temps pouvez-vous écouter
Le signet du cœur tombe à la quatrième semaine de grossesse. En une semaine, l'échographie transvaginale peut détecter des contractions du myocarde. Un examen échographique avec une sonde abdominale peut être réalisé à la huitième semaine. S'il n'y a pas de processus contractiles du myocarde à ce moment, nous pouvons conclure que la grossesse s'estompe.
Chaque domaine de la santé devrait avoir. Ressources humaines. Assurer la qualité et l'équité de ces études. Abréviations standard pour l'examen morphologique fœtal. Défaut de coupe transvenriculaire. Ventriculomégalie-hydrocéphalie. Arnold-Chiari, Encéphalocèle, Inflammation des leptomènes incohérents.
Lésion cérébrale destructrice. Anévrisme de la veine galénique Insuffisance cardiaque possible. Membres associés avec dysplasie squelettique. associés à des syndromes. Association avec d'autres malformations et syndromes. Associé à l'holoproencéphalie et à la chromosomopathie.
Après la formation, le cœur se contracte avec une fréquence de 110 à 130 battements, puis le nombre augmente considérablement à 170-190 (le pic tombe la huitième semaine), et après cela, le cœur bat à nouveau chez le fœtus diminue à 120-160 par minute et ne changent pratiquement pas jusqu'à la livraison.
L'écoute du rythme cardiaque à l'aide d'un stéthoscope n'est possible qu'à partir de la vingtième semaine, ceci n'est disponible que pour les médecins expérimentés. Vous pouvez écouter indépendamment comment le cœur du bébé bat déjà à la trentième semaine.
Associée à la chromosomopathie, l'holoproencéphalie. Les syndromes. Classification cardiaque malformations congénitales poches Cœur Droit Cœur Gauche Autre. Coeur 4 Chambres anormales 60% de cardiopathie. Cardiomyopathie septique. Cardiopathies avec asymétrie des cavités.
Anomalie d'Ebstein, dysplasie trivalente Insertion anormale du septum et des valves postérieures. Mortalité 35% intra-utérine. Par la suite, la survie à l'hypoplasie est de 90 %. La survie est de 90% et ne nécessite généralement pas de CIA immédiate. Double sortie vers le ventricule droit. Anomalies conotrubales.
Tumeur ischémique du cœur Rhabdomyome Tératome. Mouvements respiratoires adéquats dans l'espace thoracique Fluide intrapulmonaire qui sert à étirer les espaces aréolaires. Isolé par résolution spontanée de 25 %. Pas de thérapie létale. Paroi abdominale Y a-t-il une membrane terminale ? Connexion du cordon avec un défaut? Quels organes sont éviscérés ? Y a-t-il d'autres blessures associées?
Diagnostic du FEM
La détection du syndrome "balle de golf" est réalisée par ultrasons. Après cela, il est conseillé de visiter une échographie 3D supplémentaire, et le médecin traitant peut également référer la femme enceinte pour une échocardioscopie fœtale. Le plus souvent, cette étude est prescrite:
Ombilical sans infection chromosomique du foie associée à une cardiopathie, une insuffisance rénale, digestive. Paroi abdominale. Syndrome du cordon court. Détérioration de la paroi ventrale affectant l'abdomen et la poitrine. La tige est attachée au placenta. Elle est associée à des malformations. Il n'est pas associé à une chromosomie. Fatalité.
Obstruction intestinale du tractus gastro-intestinal. Tractus gastro-intestinal du kyste hépatique abdominal de la duplication intestinale mésentérique ovarienne. Artère ombilicale unique 2-1%. Trouble pelvien pallaire et anomalies vasculaires associées. Elle est associée à 50 % de chromosomopathie, à une maladie cardiaque ou à un syndrome.
- femmes enceintes de plus de 35 ans;
- si sur début de mandat la mère avait des maladies infectieuses;
- si une femme enceinte (ou des proches) a des pathologies cardiaques ou un diabète sucré;
- après détection de pathologies dans la région cardiaque lors d'une échographie planifiée;
- avec un retard dans le développement du fœtus et sa taille;
- lors de la détection de marqueurs indiquant des anomalies chromosomiques.
Un foyer hyperéchogène dans le ventricule gauche du cœur fœtal peut être examiné par échocardioscopie pendant une période de 18 à 28 semaines, après quoi il ne sera pas possible de procéder à un examen complet, car la taille de l'enfant sera trop grande pour être qualitativement examiner la taille et l'état de son cœur.
La forme périnatale associe un oligoamnios de mauvais pronostic. Gros rein exogène et homogène. Chlorure de sodium glomérulaire Osmolarité. Classification des dysplasies squelettiques. Auparavant, il existait une classification clinique et radiologique. Ostéochondrodysplasie : anomalies de la formation du cartilage, de la croissance osseuse et du développement non létal.
Système musculo-squelettique Quand faut-il suspecter une affection musculo-squelettique ? Squelette du crâne et larves de la face du système musculo-squelettique. Aplatissement de l'arête nasale. Holoproencéphalie, méningocèle, encéphalocèle, microcéphalie chromosomique. Turner, Dysgénésie clonale Hygroma kystique Hernie diaphragmatique Génitale. Anesthésie rénale, dysplasie rénale, exstrophie Vessie, Meckel-Gruber, ventre de prune, uretères. Changements dans la centrale système nerveux. Vraisemblablement associé à un déficit de dégradation fœtale.
Indicateurs de norme d'échocardioscopie
Lors de l'examen, toutes les cavités du cœur sont mesurées. Normalement, ces indicateurs doivent se situer dans la plage :
- la longueur du ventricule droit - 0,5-1,75 cm;
- largeur du ventricule droit - 0,4-1,1 cm;
- la longueur du ventricule gauche - 0,9-1,8 cm;
- largeur du ventricule gauche - 0,44-0,89 cm;
- le rapport des indicateurs de la largeur du ventricule gauche à droite - 0,45-0,9 cm;
- la bouche de l'aorte - 0,3-0,52 cm;
- la bouche de l'artère pulmonaire - 0,3-0,5 cm;
- ouverture mitrale - 0,35-0,6 cm;
- ouverture tricuspide - 0,3-0,63 cm;
- le nombre de battements de coeur - 140-160 battements / minute.
Problèmes gastro-intestinaux. Dysplasie squelettique Races des reins. Troubles du rythme et coarctation de l'aorte pulmonaire. Echo-morphologie et maladies chromosomiques. L'hypoplastie nasale est absente. Examen échographique morphologique systématique. Abréviations standard pour l'évaluation biométrique fœtale.
Plan de coupe passant par l'union du système porte avec la veine ombilicale. La diaphyse n'inclut pas le réflexe cartilagineux L'épiphysaire distal. Abréviations standard pour évaluer les adaptations fœtales. Emplacement et connexion avec le cou. Facteurs influant sur les indicateurs de développement malformatif Méthodologie d'évaluation - organisation. Facteurs facteurs techniques selon les patients et le fœtus. facteurs anormaux. Facteurs, niveau de formation et expérience en échographie.
La taille du cœur fœtal a ses propres indicateurs et diffère considérablement de la taille d'un adulte, car tous les organes correspondent à la taille du corps. La pathologie du cœur lors d'un tel examen est toujours détectée, vous ne devez donc pas vous inquiéter du manque de professionnalisme de l'échographiste si le diagnostic n'est pas confirmé ou si le médecin dit que cela ne constitue pas une menace pour l'enfant.
Diagnostic échocardiographique des tumeurs cardiaques primaires chez le fœtus. Diagnostic échocardiographique des tumeurs primitives du cœur fœtal. Cardiocentre pédiatrique "William Soler". centre national génétique médicale. Professeur agrégé du Département de pédiatrie. Six tumeurs cardiaques ont été identifiées, représentant 0,3 % des cas examinés. Cinq correspondaient à des rhabdomyomes et un à un myxome auriculaire droit. La plupart ont des voies d'entrée ou de sortie bloquées. Une arythmie a été observée dans un cas.
Mots clés : diagnostic prénatal, tumeurs cardiaques, sclérose tubéreuse, rhabdomyomes, conseil génétique. Cinq d'entre eux étaient des rhabdomyosarcomes, ainsi que des fibromes auriculaires. Grand blocus des voies d'entrée et de sortie. Dans le cas il y avait une arythmie.
Que faire lorsqu'un FEM est identifié
GEF dans le cœur du fœtus implique la nomination d'examens supplémentaires programmés par le médecin. Ceux-ci inclus:
- Échographie du cœur de l'enfant avec dopplerographie;
- CTG (cardiotocographie);
- 3D ou
Si les méthodes de diagnostic effectuées n'ont pas réfuté la présence de pathologies cardiaques (c'est-à-dire lorsqu'il existe des marqueurs pathologiques dans le sang et que ces signes sont confirmés par échographie), il est recommandé de consulter un spécialiste en génétique.
Mots clés : diagnostic prénatal, tumeurs cardiaques, sclérose tubéreuse, rhabdomyomes, recommandations génétiques. Au cours des 25 dernières années et en conséquence du développement accéléré prénatal 1-3 et l'échocardiographie post-partum, 4 tumeurs cardiaques sont plus fréquentes. 2, 4-6 Au cours de cette période, le diagnostic est passé de 0,06 % à 0,32 %. 4, 6.
Le diagnostic échographique prénatal a montré que le rhabdomyome parmi les tumeurs cardiaques primitives est le plus courant et représente 80 % de ces tumeurs. 4, 6. Le but de cette étude était d'analyser le comportement des tumeurs cardiaques primaires chez le fœtus dans deux différentes périodes depuis 20 ans.
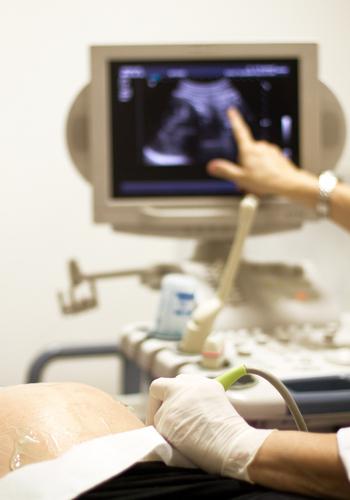
Une telle étude est une étape très sérieuse, car elle porte grand danger fausse couche ou grossesse qui s'estompe. Par conséquent, clôturer ou liquide amniotique nécessaire que dans les cas les plus extrêmes.
La pathologie du cœur peut être insignifiante, alors le généticien ne se référera pas à un diagnostic aussi dangereux. Cependant, lors de la confirmation du diagnostic par échographie volumétrique, il est préférable de consulter un professionnel sur le danger du GEF pour la vie du bébé.
Le diagnostic échocardiographique a ensuite été confirmé par une étude autopsique, à l'exception d'un cas associé à une maladie cardiaque, qui est décédé des suites de cette dernière, et le refus de la famille a empêché une autopsie. L'âge de la mère était très variable : de 14 à 26 ans, avec une moyenne de 24,5 ans.
Du point de vue de l'hémodynamique, la plupart des tumeurs étaient difficiles: la zone d'entrée d'un ventricule, à la fois les ventricules et les ventricules du ventricule droit. Table. Caractéristiques des tumeurs cardiaques fœtales. L'arythmie s'est manifestée dans un cas, dans lequel de multiples tumeurs intracardiaques sont apparues, occupant indifféremment à la fois les ventricules, le septum et les valves auriculo-ventriculaires. Les petites tumeurs étaient généralement accompagnées d'une bradyarythmie sévère comme l'ont rapporté Cha-Ban et al.19.
Focalisation hyperéchogène dans le ventricule gauche du cœur fœtal : causes
La survenue d'un foyer échogène dans le cœur d'un enfant peut être due à la minéralisation des vaisseaux du muscle cardiaque, caractéristique individuelle cardiaque (dans lequel se trouve un septum supplémentaire dans le cœur sous la forme d'une petite corde) ou des pathologies chromosomiques, en particulier le syndrome de Down.
Le cas #1 a montré une tumeur septale ventriculaire qui occupait la majeure partie de la cavité ventriculaire droite et provoquait une obstruction partielle de sa lumière. Le Doppler continu montrait une régurgitation tricuspargique par écho couleur et un gradient de pression de 48 mmHg. Au niveau de son écoulement. La localisation de la tumeur se situait principalement au niveau du septum interventriculaire, ainsi 5 des 6 cas étudiés ont été identifiés.
Chez un fœtus, la tumeur occupait l'oreillette droite et était très mobile : lors de la diastole, le ventricule droit s'est déplacé pour revenir dans la cavité auriculaire en systole. Il s'agissait d'un myxome, une tumeur très rare et, selon 5 autres, encore non diagnostiquée chez le fœtus.
Le fœtus se développe très rapidement au fil des semaines et son corps et les systèmes vitaux du corps s'améliorent encore plus. C'est pourquoi vous devez surveiller régulièrement l'état du fœtus, ce qui vous permettra de détecter à temps problèmes possibles développement ou les prévenir avant l'apparition des premiers symptômes.
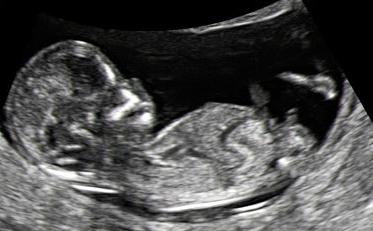
D'un point de vue histopathologique, le diagnostic de rhabdomyome a été confirmé dans 4 cas, et l'autre cas correspondait à un myxome auriculaire droit, comme déjà noté. L'échocardiogramme était diagnostique dans tous les cas avec une sensibilité de 100% et une spécificité de 99,8%. La figure 2 montre les caractéristiques échocardiographiques d'un rhabdomyome, et la figure 3 montre Caractéristiques myxomes.
Toutes les grossesses ont été interrompues, sauf une, sur décision du couple. Ce fut le cas non. 3, qui est également associée à des maladies cardiaques et à une bradycardie sévère. Sur 5 patients atteints de rhabdomyomes, 4 avec des critères histopathologiques et d'autres avec des critères cliniques et échocardiographiques, ce dernier n'a été retrouvé qu'avec une sclérose tubéreuse se présentant au suivi postnatal avec des lésions cutanées et des manifestations neurologiques compatibles avec ce diagnostic.
En présence de marqueurs chromosomiques pathologiques dans le sang de la mère, la présence d'anomalies du développement chez l'enfant est finalement confirmée. Dans ce cas, les parents doivent décider si des examens complémentaires ou une interruption de grossesse sont nécessaires.
Conséquences du diagnostic pour l'enfant
Ce n'est que dans un petit pourcentage de cas qu'une corde supplémentaire du ventricule gauche chez un enfant peut entraîner l'une ou l'autre des autres pathologies. Mais pour cela, la simple présence du syndrome de la "balle de golf" ne suffit pas, il faut confirmer avec précision le danger par un prélèvement de liquide amniotique ou de sang du cordon ombilical et la présence de marqueurs pathologiques après diagnostic sanguin, indiquant la présence de anomalies chromosomiques chez le fœtus.
Lors de l'examen échographique, aucun des patients n'avait histoire de famille les tumeurs cardiaques ou les manifestations cutanées, neurologiques, rénales ou pulmonaires de la sclérose tubéreuse. Les tumeurs cardiaques primaires chez le fœtus sont souvent multiples et peuvent être trouvées indistinctement n'importe où dans la cavité cardiaque. 3 Dans ce cas, la moitié des 6 cas étaient des multiples, ce qui est très un facteur important pour le diagnostic étiologique du rhabdomyome, 3, 4, car les myxomes et les fibromes sont invariablement des tumeurs solitaires et les autres tumeurs cardiaques primitives ne sont observées qu'occasionnellement. 6, 18.
Un foyer hyperéchogène dans le ventricule gauche du cœur fœtal est une constatation échographique qui est généralement détectée lors de la deuxième échographie programmée. Sur le ce moment son apparence est décrite dans de nombreux fruits. Les experts estiment qu'il peut s'agir à la fois d'une variante de la norme et - uniquement dans le contexte de marqueurs identifiés d'anomalies chromosomiques - indiquer une pathologie grave.
Que signifie une focalisation hyperéchogène dans le cœur du fœtus ?
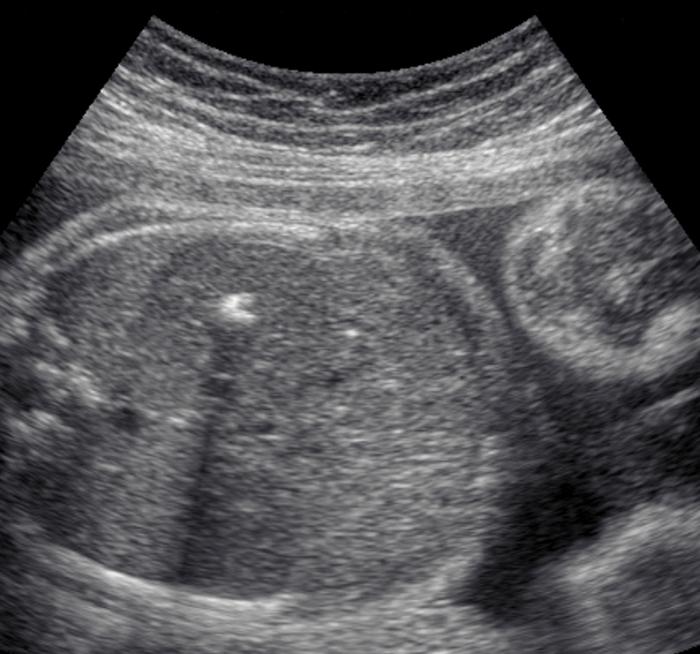
Ce phénomène est également appelé des termes tels que "balle de golf" ou "balle de golf (balle de golf)". On peut le voir sur la photo du fœtus comme point blanc dans la région du coeur. Lorsque le sonologue l'examine dans une certaine section et mise à l'échelle, il voit une formation arrondie qui rebondit en rythme avec les contractions du myocarde (d'où le nom).Un foyer hyperéchogène dans le cœur fœtal signifie qu'à l'endroit où il se trouve, il y a eu un épaississement des structures myocardiques. Il pourrait être:
- dépôts de sel (généralement des sels de calcium)
- une corde supplémentaire ou une autre anomalie du développement qui n'interfère généralement pas avec la fonction cardiaque normale
- signe d'une pathologie chromosomique.
En cas de détection d'un seul de ces phénomènes, ne vous inquiétez pas: s'il s'agit du dépôt de sels, il disparaît généralement au troisième trimestre ou à la naissance.
La corde supplémentaire (c'est-à-dire le tissu fibreux qui va des valves aux ventricules), selon la plupart des médecins, ne présente pas de danger pour la vie et la santé et ne constitue pas une menace pour le travail du système cardio-vasculaire n'affecte pas.
Le même accord supplémentaire peut être la source de souffles cardiaques retrouvés plus tard chez votre bébé.
Cela n'affecte pas la santé, mais vous devez être constamment observé par un cardiologue. Cela est nécessaire pour qu'en cas d'autres problèmes de circulation sanguine, que le bruit constant peut empêcher le pédiatre de reconnaître, ils puissent toujours être détectés.
Mais si des marqueurs d'anomalies chromosomiques ont déjà été détectés chez vous (déterminés par un test sanguin, généralement prescrit par un généticien), un foyer hyperéchogène peut ne pas être une anomalie aussi simple.
Cela peut être la preuve de maladies chromosomiques graves, en particulier le syndrome de Down.
Que faire si un enfant a une "balle de golf"
Le diagnostic invasif, comme la cordocentèse (une ponction du cordon ombilical suivie d'un prélèvement sanguin) ou l'amniocentèse (une ponction du sac amniotique avec prélèvement d'une petite quantité de liquide amniotique) est une étape sérieuse. Premièrement, si une telle pathologie échographique est détectée, les étapes suivantes doivent être suivies:
- Échographie avec reconstruction volumétrique, c'est-à-dire (ou)
- () avec dopplerographie
- (KTG)
Si toutes ces études ne donnent pas un résultat rassurant sans ambiguïté, il faut se tourner vers la génétique. Uniquement dans le cas le plus extrême :
- si des marqueurs dangereux sont trouvés dans le sang,
- il existe d'autres signes échographiques de pathologie,
à sa suggestion, il vaut la peine d'effectuer les procédures invasives indiquées ci-dessus.
Combien de temps pouvez-vous écouter le rythme cardiaque du fœtus
Le cœur est pondu à 4 semaines. Le premier battement cardiaque fœtal à l'échographie peut déjà être déterminé. Ça peut être fait. capteur de fréquence cardiaque peut être enregistré une semaine ou deux plus tard. Si lors d'une échographie réalisée le ou plus tard, les contractions du myocarde ne sont pas visualisées, cela indique une grossesse manquée.
Le nombre de contractions du muscle cardiaque au cours de la première période devrait être de 110 à 130 par minute. Dans la période de 8 semaines, ils devraient déjà être d'environ 170-190 par minute. Lors d'une échographie effectuée sur, le rythme cardiaque fœtal est entendu à une fréquence de 120-160 par minute. Cette fréquence est maintenue jusqu'au moment de la livraison.
Cette détection précoce du rythme cardiaque fœtal n'est audible qu'à l'échographie. Même le médecin le plus expérimenté peut le faire avec un stéthoscope de 20 à 22 semaines. Les membres de votre famille peuvent écouter comment ça bat seulement à partir de 30 semaines.
Échocardioscopie fœtale
Elle est réalisée selon les indications suivantes :
- future maman de plus de 35 ans
- elle souffre de diabète
- la femme avait été atteinte d'une sorte de maladie infectieuse au début
- l'échographie conventionnelle a révélé une pathologie du coeur
- selon la fœtométrie, la taille du fœtus est en retard par rapport à l'âge gestationnel
- une malformation cardiaque a été découverte chez la femme enceinte elle-même, ses proches ou ses enfants plus âgés
- avec des marqueurs détectés de maladies chromosomiques.

A quel moment faut-il faire une échographie du cœur fœtal ? Cela ne se fait qu'à partir de la 18e semaine de grossesse.
Après 28 semaines, l'étude est non informative, car l'évaluation des résultats de l'étude est difficile en raison de la faible quantité de liquide amniotique et grandes tailles l'enfant lui-même.
L'échocardioscopie évalue les différentes tailles des cavités du cœur et des valves, son remplissage et sa contractilité. Ils diffèrent des mesures de cet organe chez un adulte, car le fœtus a une zone corporelle complètement différente.
Donc, cela est représenté par de telles normes (en centimètres):
- largeur du ventricule droit (RV) : 0,4-1,10
- largeur du ventricule gauche (LV): 0,45-0,9
- Rapport de largeur LV/RV : 0,9-1,15
- Longueur VG : 0,9-1,8
- longueur de la prostate : 0,5-1,75
- bouche aortique : 0,3-0,52
- diamètre du foramen tricuspide : 0,32-0,65
- diamètre de l'orifice mitral : 0,36-0,63
- embouchure de l'artère pulmonaire : 0,28-0,5
- fréquence cardiaque : 140-160 par minute.
Le prix d'une telle étude : 1900 - 2600 roubles.
Ainsi, un foyer hyperéchogène dans le ventricule gauche du cœur fœtal est un phénomène ultrasonore, qui le plus souvent ne signifie pas une pathologie. La détection d'une telle ombre acoustique nécessite un examen supplémentaire supplémentaire de manière planifiée. La nomination de diagnostics invasifs sans indications sérieuses dans ce cas est déraisonnable.