Was ist Stickoxid im menschlichen Körper? Stickoxid im menschlichen Körper. Mögliche Gefahren der Stickoxidunterdrückung
Stickstoffmonoxid ist ein aus Stickstoff (N) und Sauerstoff (O) gebildetes Signalmolekül, das wörtlich NO genannt wird. Stickstoffmonoxid spielt eine wichtige Rolle bei der Gefäßentspannung (Blutdruckregulierung, erektile Dysfunktion), der Immunantwort, Entzündungen, der antithrombotischen Aktivität und der Gedächtnisbildung.
Auch bekannt als: NEIN
Biologische Bedeutung
Struktur
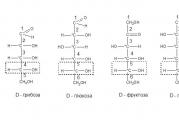
Stickstoffmonoxid (im Folgenden NO – siehe Abbildung unten) ist ein kleines Signalmolekül, das aus der Aminosäure L-Arginin durch eine Familie von Stickstoffmonoxid-Synthetasen synthetisiert wird, darunter eNOS (endothelial, NOS-III), iNOS (induzierbar, NOS-II) und nNOS (neuronal, NOS-I). Diese Familie von Enzymen fungiert als Dimere mit einer Vielzahl von Cofaktoren, darunter Tetrahydrobiopterin, Flavinadenindinukleotid (FAD), Flavinmononukleotid (FMN), Eisen und Zink. Während die Regulierung und Modulation jeder Isoform erheblich variiert, beschleunigen alle Isoformen die Reaktion von L-Arginin mit NADPH und Sauerstoff zur Bildung von NO, Citrullin und NADP (Knowles und Moncada (1994); Marletta (1994).
Wie überträgt Stickoxid ein Signal?
Die Erklärung der Wirkung von Stickstoffmonoxid als Signalgasmolekül führte 1998 zur Verleihung des Nobelpreises für Psychologie/Medizin, da erstmals festgestellt wurde, dass das Gasmolekül von einer Zelle produziert und sofort auf andere Zellen übertragen wird und fungiert dann als Signalmolekül in Zellen. Beispielsweise wird von eNOS in Endothelzellen produziertes NO zu benachbarten glatten Muskelzellen transportiert, wo es durch Aktivierung der löslichen Guanylatcyclase eine Reaktionskaskade auslöst, die die Produktion von zyklischem GMP beschleunigt. Ein Anstieg der cGMP-Spiegel führt zur Aktivierung der Proteinkinase G (PKG), die wiederum die Phosphatasen der Myosin-Leichtkette (MLC) phosphoryliert (und sie dadurch aktiviert). Die aktivierte MLC-Phosphatase wiederum dephosphoryliert MLC, was zu einer Entspannung der glatten Muskelzellen und damit einer Gefäßentspannung führt. Stickoxid signalisiert, indem es seinen Rezeptor, den löslichen Guanylylcyclase-Rezeptor, stimuliert und die zellulären Spiegel eines Signalmoleküls namens zyklisches Guanidinmonophosphat (cGMP) erhöht. Zu den weiteren Teilnehmern an der Regulierung des Gefäßtonus gehört die Phosphodiesterase-Familie (PDE 1–11), die die Hydrolyse von cGMP zum 3'-Endprodukt beschleunigt und so die NO-vermittelte Gefäßrelaxation effektiv stoppt. Aufgrund der begrenzten Regulierung der eNOS- und NO-Produktion ist es schwierig, die Gefäßentspannung durch Beeinflussung der eNOS-Aktivität zu modulieren. Aufgrund der physiologischen Bedeutung von PDEs für die Kontrolle des cGMP-Spiegels sind sie zu einem beliebten Ziel geworden, wenn es um die Entspannung von Blutgefäßen und den Blutfluss geht. Zu den Behandlungen gehören Medikamente wie Viagra, Cialis und Levitra, die alle PDE5 hemmen, das insbesondere in den glatten Muskelzellen im Schwellkörper des Penis exprimiert wird. Da die Hemmung dieser Enzyme zur Akkumulation von cGMP führt, wird es deutlich möglich, die gefäßentspannende Wirkung von NO zu verstärken. Phosphodiesterasen sind negative Regulatoren von cGMP und cAMP (sie hydrolysieren diese Moleküle). Während nicht alle PDE-Enzyme auf die cGMP-induzierten Wirkungen von NO auf die Guanylatzyklase abzielen können, verfügen einige wenige über die Fähigkeit, die NO-Signalübertragung durch den Abbau eines wichtigen Signal-Botenmoleküls (cGMP) zu kontrollieren.
Oxidationspotential
NO kann theoretisch in ein Molekül namens Peroxynitrat (OONO-) zerfallen, das das Ergebnis der Reaktion von NO mit Superoxidanionen (O2-) ist. OONO- fungiert auch als reaktives Signalmolekül, obwohl das Endergebnis die Bildung einiger Strukturen ist, die für den Körper negativ sind; OONO- kann Aminosäuren nitrosylieren (eine Stickstoffgruppe spenden), um Verbindungen wie 3-Nitrotyrosin oder S-Nitrosocystein zu bilden, Proteincarbonyle zu bilden oder Phospholipide, die mehrfach ungesättigte Fettsäuren (PUFAs) enthalten, zu nitrosylieren. In diesem Sinne kann Stickoxid von Superoxid als Substrat zur Bildung reaktiver Verbindungen genutzt werden, die sich negativ auf die Gesundheit auswirken, obwohl NO vergleichsweise vorteilhaft für den Körper ist. Stickstoffmonoxid kann (durch Kombination mit Superoxidradikalen) in die Form von Peroxynitrat umgewandelt werden, das dann eine Vielzahl von Molekülen bilden kann, die mit ungesunden Zuständen in Verbindung gebracht werden und vermutlich mit Pathologien in Zusammenhang stehen.
Pharmakologie
Additiv Stickstoffmonoxid
NO, das im Körper synthetisiert und anschließend ins Blut freigesetzt wird, hat eine Halbwertszeit von 5 Sekunden oder weniger, und einige Komplexe können in vitro hergestellt werden, um die Halbwertszeit zu Forschungszwecken auf etwa 445 Sekunden zu erhöhen. Diese kurzen Halbwertszeiten weisen auf den schnellen Abbau des Stickoxidmoleküls in seine Bestandteile (Stickstoff und Sauerstoff) hin, und die ordnungsgemäße Lagerung von NO kann die Haltbarkeitsdauer verlängern, die bei Verwendung von Mylar-Ballons nachweislich nur bis zu 5 Tage beträgt den Zusammenbruch verlangsamen. Aufgrund seiner geringen Persistenz außerhalb des Körpers wird Stickstoffmonoxid grundsätzlich nie als Nahrungsergänzung verwendet, sondern es werden Verbindungen verwendet, die lange genug im Blut verbleiben können, um kontinuierlich neues NO zu produzieren. Stickstoffmonoxid ist grundsätzlich instabil und hat eine kurze Halbwertszeit; Es hat unmittelbare Vorteile, ist aber als Ergänzung oder allein wertlos. Eine NO-Ergänzung erfordert andere Verbindungen, die das interne Stickoxid-Produktionssystem beeinflussen.
Physiologie
Das Herz-Kreislauf-System
Stickstoffmonoxid hängt mit der Entspannung der Gefäßmuskulatur zusammen, was der Mechanismus ist, der den kardioprotektiven Wirkungen von Stickstoffmonoxid (durch Senkung des Blutdrucks) zugrunde liegt.
Neuronale Aktion
Stickstoffmonoxid moduliert Ionenkanäle, die angeborene Erregbarkeit, vermittelt synaptische Plastizität und kann Zellmembranen durchdringen. Neuronale Stickoxidsynthase (nNOS) ist in der Lage, mit einem Protein namens PSD95 ein Dimer zu bilden, und dieser Komplex ist ein positiver Regulator von Depressionen, da die Hemmung der nNOS-PSD95-Wechselwirkung antidepressive Wirkungen hat. Dieser Komplex wird nach Aktivierung des NMDA-Rezeptors aktiviert.
Zusatzstoff
Stickstoffmonoxid-Donatoren
Einige Nahrungsergänzungsmittel, die auf die NO-Produktion abzielen, stellen lediglich Stickstoffquellen bereit, die das NOS-Enzym zur Produktion von NO nutzen kann. Arginin ist der Standard-NO-Donor in Nahrungsergänzungsmitteln, wobei Citrullin die bioverfügbarste Form von Arginin darstellt. Weitere NO-Donatoren sind S-Nitrosoglutathion (endogen produziert) oder zwei Klassen von N-Diazeniumdiolaten oder S-Nitrosothiolen, wobei letztere endogenes S-Nitrosoglutathion enthalten. Einige Verbindungen versorgen das Enzym einfach mit Stickstoff, um Stickoxid zu produzieren.
Stickstoffmonoxid (NO) ist ein gasförmiges Signalmolekül des menschlichen Körpers und einer der starken Vasodilatatoren (Stickoxid für die Potenz).
Gerade weil es die Blutzirkulation im gesamten menschlichen Körper verbessert, werden Stickoxid-Booster oft als Nahrungsergänzungsmittel vor dem Training von Gewichthebern und anderen Sportlern verwendet, die von dieser Steigerung der Blutzirkulation in ihrer gewählten Sportart profitieren.
Das Auftreten des „Pump“-Effekts vor dem Training ist jedoch bei weitem nicht der einzige Vorteil einer Erhöhung des Stickoxidspiegels im menschlichen Körper:
A) Stickstoffmonoxid eignet sich hervorragend zur Vorbeugung von Herz-Kreislauf-Erkrankungen, da es die Arterienwände entspannt, die Blutgefäße erweitert und die Durchblutung verbessert.
B) NO verbessert die Gehirnfunktion und reduziert den kognitiven Verfall, indem es die Durchblutung des Gehirns deutlich erhöht und als Ersatz-Neurotransmitter zwischen Nervenzellen fungiert.
V) Stickstoffmonoxid ist eines der Hauptelemente, die für Erektionen verantwortlich sind, und ohne das Molekül könnten Sie es einfach nicht haben. Einfach ausgedrückt: Je mehr Stickoxid Sie in Ihrem Körper haben, desto stärker ist Ihr „Liebesinstrument“.
D) Ein hoher Stickoxidspiegel kann Ihre Trainingsleistung erheblich verbessern, denn wenn Ihre Venen erweitert und die Durchblutung erhöht werden, erhalten Ihre Muskeln mehr Sauerstoff und Nährstoffe. Aus dem gleichen Grund verkürzt NO die Muskelregenerationszeit.
Einfach ausgedrückt sorgt Stickstoffmonoxid dafür, dass der Körper effizienter arbeitet, indem es Sauerstoff, Nährstoffen und roten Blutkörperchen ermöglicht, schneller die Gewebe und Zellen zu erreichen, die sie benötigen.
Tatsächlich erhielt das Forscherteam, das die gefäßerweiternde und herzschützende Wirkung von Stickstoffmonoxid entdeckte, bereits 1998 einen Nobelpreis. Das NO-Molekül ist also eine sehr wichtige Sache, insbesondere für Männer ...
In den Artikeln bewerte ich dieses Molekül als das zweitwichtigste Molekül im Körper, ein Element, das direkt nach Testosteron optimiert werden muss.
Glücklicherweise ist die natürliche Erhöhung Ihres Stickoxidspiegels ganz einfach und auch mit einem kleinen Budget möglich.
Oft können sehr schnell Ergebnisse erzielt werden. Beispielsweise können Sie Ihren Stickoxidspiegel an einem Tag verdoppeln, indem Sie einfach den folgenden Tipp Nr. 1 befolgen (ich verwende spezielle Klebestreifen, um meine Werte zu Hause zu überwachen).
Nachdem Sie nun wissen, was Stickoxid ist und warum es so wichtig ist, finden Sie hier 20 Möglichkeiten, Ihren NO-Wert auf natürliche Weise zu erhöhen:
 Wenn Sie Lebensmittel essen, die natürliche Nitrate enthalten, wandeln Bakterien auf Ihrer Zunge diese in Nitrite um ...
Wenn Sie Lebensmittel essen, die natürliche Nitrate enthalten, wandeln Bakterien auf Ihrer Zunge diese in Nitrite um ...
Und sobald Sie Ihre Nahrung schlucken, wandeln Bakterien in Ihrem Darm Nitrite in Stickoxid um.
Dieses Phänomen – Sie haben es erraten – erhöht den Stickoxidspiegel im Körper, je nachdem, welche Dosis Sie zu sich nehmen (je mehr Nitrate Sie essen, desto mehr Stickoxid produzieren und verarbeiten Ihre Zunge und Ihr Darm).
Glücklicherweise sind nitratreiche Lebensmittel leicht zu bekommen und relativ günstig ...
...Hier ist eine Liste einiger bekannter Lebensmittel, die mit natürlich vorkommenden Nitraten beladen sind:
Spinat, Rüben, Sellerie, Salat, Eisbergsalat, Karotten, Petersilie, Kohl, Radieschen, Kräuter usw.
beachten Sie: Einige sprechen von den Gefahren von Nitraten, angeblich werden sie im Körper in krebserregende Nitrosamine umgewandelt. In Wirklichkeit haben Sie jedoch nichts zu befürchten. Lesen Sie einfach den hervorragenden Artikel von Dr. Kessers zu diesem Problem. Um besonders sicher zu sein, gibt es Vitamin C, das die Möglichkeit einer Umwandlung in Nitrosamine vollständig blockiert.
 Traubenkernextrakt (GSE) ist ein Extrakt, der aus den Kernen von Weintrauben gewonnen wird.
Traubenkernextrakt (GSE) ist ein Extrakt, der aus den Kernen von Weintrauben gewonnen wird.
Der Extrakt selbst eignet sich hervorragend zur Unterstützung der Testosteronproduktion, da er einer der wenigen natürlichen Stoffe ist, die die Umwandlung von Testosteron in Östrogen blockieren können. Mit anderen Worten: ECV ist ein starker Aromataseblocker (mehr dazu hier).
Darüber hinaus ist Traubenkernextrakt eine hervorragende Möglichkeit, den Stickoxidspiegel zu erhöhen...
Humanstudien haben gezeigt, dass ECV den Blutdruck und die Herzfrequenz senkt, und Tierstudien zeigen, dass es die natürliche Stickoxidsynthese des Körpers aktiviert und den NO-Spiegel um bis zu 138 % erhöht, wenn es in Dosen von 100 mg/kg eingenommen wird. (Forschung, Forschung, Forschung, Forschung, Forschung, Forschung)
Das Problem bei ECV besteht darin, dass man allein durch den Verzehr von Weintrauben nicht genug von den Wirkstoffen (Procyanidinen) aufnehmen kann und die meisten Nahrungsergänzungsmittel auf dem Markt auch schwach sind. Das einzige ECV-Ergänzungsmittel, das ich ehrlich empfehlen kann, ist dieser Extrakt.
3. Vitamin C + Knoblauch
 Es ist eine wohlbekannte medizinische Tatsache, dass Vitamin C die Produktion von Stickoxid im Körper erhöht und außerdem die Moleküle schützt.
Es ist eine wohlbekannte medizinische Tatsache, dass Vitamin C die Produktion von Stickoxid im Körper erhöht und außerdem die Moleküle schützt.
Andererseits enthält Knoblauch, der mit Nitraten beladen ist, auch eine Verbindung namens Quercetin, die in einer Reihe von Studien mit erhöhten NO-Werten in Verbindung gebracht wurde (mehr zu Quercetin später in diesem Artikel).
Einige Studien haben gezeigt.
Aus diesem Grund führte ein Forscher namens Adam Musa eine Studie durch, in der er Probanden 10 Tage lang etwas Vitamin C (2 g) zusammen mit 4 Kapseln Knoblauch (6 mg Allicin und 13,2 mg Alliin) verabreichte, um zu sehen, ob es gesundheitliche Vorteile oder eine Wirkung hatte auf ihren Blutdruck und/oder Stickoxidspiegel...
... Die Ergebnisse waren sehr beeindruckend:
- Die endotheliale Stickoxidproduktion stieg um unglaubliche 200 %.
- Der durchschnittliche systolische Blutdruck sank von 142 mm auf 115 mm, mehr als mit den meisten Medikamenten erreichbar ist.
- Der diastolische Blutdruck sank von durchschnittlich 92 mm auf 77 mm.
Wenn Sie also das nächste Mal in Ihrem örtlichen Geschäft über den Kauf eines Blutdruckmedikaments im Wert von 1.500 US-Dollar nachdenken, denken Sie daran, dass Sie mit den altbewährten Knoblauchkapseln (oder Knoblauchzehen) und Vitamin C bessere Ergebnisse und einen Pumpeffekt erzielen können =).
 L-Citrullin ist eine Aminosäure, die in den Nieren zu L-Arginin umgewandelt wird.
L-Citrullin ist eine Aminosäure, die in den Nieren zu L-Arginin umgewandelt wird.
L-Arginin wird dann durch das Enzym Stickstoffmonoxid-Synthase (NOS) in Stickstoffmonoxid umgewandelt. Das bedeutet, dass die Ergänzung mit L-Citrullin eine direkte Möglichkeit ist, den NO-Spiegel auf natürliche Weise zu erhöhen (bewiesen, bewiesen).
Warum nehmen Sie dann nicht ein Nahrungsergänzungsmittel mit fertigem L-Arginin ein?
Antwort: Aus irgendeinem seltsamen Grund erhöht L-Citrullin den Argininspiegel im Serum besser als L-Arginin selbst. Das bedeutet nicht, dass L-Arginin selbst nicht wirkt, sondern nur, dass Citrullin den Stickoxidspiegel aus Arginin besser steigert als aus Aminosäuren.
Sie können Citrullin durch den Verzehr von Wassermelone erhalten. Um die sichtbaren Effekte zu erzielen, wird jedoch eine Ergänzung mit der Aminosäure empfohlen. Das beste Medikament in Bezug auf die biologische Wertigkeit ist .
5. Arginin
 Wie ich oben sagte, erhöht L-Citrullin den Argininspiegel wirksamer als L-Arginin allein, was seltsam ist, aber manchmal kann der Körper auf diese Weise arbeiten (vielleicht ist das von den Nieren produzierte Arginin von höherer Qualität als das von den Nieren produzierte Arginin). Nieren). Im Labor hergestellt).
Wie ich oben sagte, erhöht L-Citrullin den Argininspiegel wirksamer als L-Arginin allein, was seltsam ist, aber manchmal kann der Körper auf diese Weise arbeiten (vielleicht ist das von den Nieren produzierte Arginin von höherer Qualität als das von den Nieren produzierte Arginin). Nieren). Im Labor hergestellt).
Auch wenn Citrullin besser wirkt, heißt das nicht, dass Arginin völlig nutzlos ist. Es bleibt der Hauptbestandteil fast aller Pre-Workout-Booster.
Einige Studien haben gezeigt, dass Arginin den Stickoxidspiegel erhöht.
Aber auch hier gilt: Citrullin. Wenn Sie Arginin ausprobieren möchten, greifen Sie zu diesem Produkt, das beides enthält. Sie können Arginin auch aus verschiedenen Lebensmitteln, wie zum Beispiel Paranüssen, aufnehmen.
6. Training
 Bewegung und ein aktiver Lebensstil haben erstaunliche Auswirkungen auf alle Aspekte des Lebens. Schließlich sind wir nicht dazu geschaffen, den ganzen Tag zu sitzen.
Bewegung und ein aktiver Lebensstil haben erstaunliche Auswirkungen auf alle Aspekte des Lebens. Schließlich sind wir nicht dazu geschaffen, den ganzen Tag zu sitzen.
Wir müssen ständig in Bewegung sein, gehen, klettern usw.
Bei praktisch allen Arten von körperlicher Betätigung (vom Gehen bis zum hektischen Krafttraining) kommt es zu einem vorübergehenden oder dauerhaften Anstieg des Stickoxidspiegels.
Wenn Sie außerdem regelmäßig ins Fitnessstudio gehen, steigt Ihre Stickoxidproduktion mit zunehmender Muskelmasse. In gewisser Weise merkt Ihr Körper, dass Ihre Muskeln mehr Blut, Sauerstoff und Nährstoffe benötigen, daher erhöht er die Stickoxidsynthese und somit steigt auch Ihr natürlicher Stickoxidspiegel ...
... Dies ist einer der Gründe, warum Bodybuilder zu viele hervorstehende Blutgefäße haben.
 Pycnogenol ist eine Extraktformel aus der Rinde von Meereskiefern, die zu 65–75 % gewichtsmäßig auf Procyanidine standardisiert ist (derselbe Wirkstoff wie Traubenkernextrakt).
Pycnogenol ist eine Extraktformel aus der Rinde von Meereskiefern, die zu 65–75 % gewichtsmäßig auf Procyanidine standardisiert ist (derselbe Wirkstoff wie Traubenkernextrakt).
Pycnogenol hat außerdem eine Reihe antidiabetischer, entzündungshemmender und antioxidativer Eigenschaften ...
Aber das wirklich Interessante an Pycnogenol, und das wurde durch viele wissenschaftliche Studien bestätigt, ist seine Wirkung als Durchblutungsbeschleuniger.
Schauen Sie sich einfach diese Studien an:
- Diese Studie ergab, dass Pycnogenol die Innenwand von Arterien entspannen kann.
- In dieser Studie verbesserten 40 mg und 120 mg orales Pycnogenol die Qualität, das Erreichen und die Dauer von Erektionen bei Patienten mit erektiler Dysfunktion (höchstwahrscheinlich aufgrund einer erhöhten Durchblutung) erheblich.
- Einige Studien haben gezeigt, dass Pycnogenol die Menge an Stickoxid erhöht, die Durchblutung verbessert und die Symptome einer venösen Leckage lindert.
Pycnogenol ist also definitiv eine interessante Verbindung. Ich persönlich habe es noch nicht ausprobiert. Obwohl ich für mich selbst bereits 2 Produkte von Healthy Origins und Twinlab ausgewählt habe.
 Es ist eine bekannte Tatsache, dass Sonnenlicht die Haut dazu veranlasst, Vitamin D zu produzieren.
Es ist eine bekannte Tatsache, dass Sonnenlicht die Haut dazu veranlasst, Vitamin D zu produzieren.
Was die meisten Menschen jedoch nicht wissen, ist, dass natürliches Sonnenlicht auch dazu führt, dass die Haut mehr Stickoxid produziert (vorausgesetzt, Sie verwenden keine Sonnenschutzmittel, die die natürliche Brillanz der Sonnenstrahlen blockieren).
Auch hierfür gibt es wissenschaftliche Belege. Forscher der Universität Edinburgh haben herausgefunden, dass Stickstoffmonoxid sofort ins Blut freigesetzt wird, wenn Sonnenlicht auf die Haut trifft ...
Sie kamen außerdem zu dem Schluss, dass Sonnenlicht die Lebenserwartung erheblich verlängern und gleichzeitig das Schlaganfallrisiko verringern kann.
„Wir vermuten, dass die Vorteile der Sonneneinstrahlung für die Herzgesundheit das Hautkrebsrisiko überwiegen. Unsere Arbeit hat uns geholfen, den Mechanismus zu verstehen, der diesen Prozess erklären könnte, und auch, warum die einfache Einnahme von Vitamin D den Mangel an Sonnenlicht möglicherweise nicht ausgleicht.“ ." .
Machen Sie sich also keine Sorgen mehr über Hautkrebs. Sonnenlicht ist für den Menschen lebenswichtig und kann nicht aus einer Flasche gewonnen werden. Darüber hinaus ist die Wahrscheinlichkeit, an einem Schlaganfall zu sterben, 80-mal höher als die Wahrscheinlichkeit, an Hautkrebs zu sterben.
 Ginseng oder „echter koreanischer Ginseng“ wird in Korea angebaut.
Ginseng oder „echter koreanischer Ginseng“ wird in Korea angebaut.
Es enthält Wirkstoffe namens „Ginsenoside“, die in ihrer Struktur Androgenen wie Testosteron sehr ähnlich sind.
Ginseng ist interessant, weil Laut verschiedenen Humanstudien erhöht es den Testosteronspiegel, erhöht den Stickoxidspiegel, verbessert die Durchblutung, fördert eine bessere Schlafqualität, entspannt die Arterien und steigert die Libido. (Studie 1, Studie 2, Studie 3, Studie 4, Studie 5, Studie 6).
Ginseng ist ein sehr beliebtes Kraut, weshalb es viele gefälschte Produkte auf dem Markt gibt. Beachten Sie auch, dass es sich hier um koreanischen roten Ginseng (Panax) handelt und nicht um eine der amerikanischen oder sibirischen Alternativen.
Eine Tierstudie legt außerdem nahe, dass Capsaicin Testosteronmoleküle bei längerem Kalorienmangel schützen kann.
Sie können Capsaicin erhalten, indem Sie Ihren Speisen etwas Cayennepfeffer (oder andere scharfe Chilischoten) hinzufügen oder ein Nahrungsergänzungsmittel einnehmen, wenn Sie keine scharfen Speisen mögen.
 Stickstoffmonoxid ist eine gefäßerweiternde Verbindung, was bedeutet, dass es die Blutgefäße erweitert und den Blutdruck senkt...
Stickstoffmonoxid ist eine gefäßerweiternde Verbindung, was bedeutet, dass es die Blutgefäße erweitert und den Blutdruck senkt...
Kaffee hingegen ist das genaue Gegenteil. Es ist ein Vasokonstriktor, das heißt, es verkleinert die Blutgefäße und erhöht auch den Blutdruck.
Darüber hinaus enthält Kaffee einen hohen Anteil an Antioxidantien, die laut dieser Studie die Synthese des Enzyms Stickoxid steigern, das Arginin in NO umwandelt.
So erhöhen die Antioxidantien im Kaffee die Menge an Stickoxid und das darin enthaltene Koffein verengt die Blutgefäße.
Daher ist Kaffeetrinken höchstwahrscheinlich weder gut noch schlecht. Außer wenn Sie entkoffeinierten Kaffee trinken, kommt es zu einem Anstieg des NO-Spiegels, es kommt jedoch zu keiner Gefäßverengung. Darüber hinaus werden Sie den durch Kaffee verursachten Anstieg des Testosteronspiegels nicht bemerken, da dieser durch Koffein verursacht wird.
 Rohkakao – und damit meine ich ungeheizten, aus den Bohnen gepressten Kakao – ist ein Superfood, das jede Menge Polyphenole und Antioxidantien enthält.
Rohkakao – und damit meine ich ungeheizten, aus den Bohnen gepressten Kakao – ist ein Superfood, das jede Menge Polyphenole und Antioxidantien enthält.
Dies ist der Grund, warum es auch die Stickoxidproduktion schnell steigert und die Innenwände der Arterien entspannt (studieren, studieren, studieren).
Tatsächlich enthält Rohkakao neben vielen anderen Antioxidantien, die den NO-Spiegel im Körper nicht erhöhen, die gleichen Bestandteile wie Pycnogenol und Traubenkernextrakt (Protocyanidin).
 Omega-3-Fettsäuren sind verdammt gesund. Dem kann ich nicht widersprechen.
Omega-3-Fettsäuren sind verdammt gesund. Dem kann ich nicht widersprechen.
Sie wirken entzündungshemmend, erhöhen die Durchblutung und den Stickoxidspiegel deutlich und reduzieren das Risiko von Schlaganfällen und Blutgerinnseln auf erstaunliche Weise.
Die Wahrheit ist, dass wir zu wenig dieser essentiellen Fettsäuren zu uns nehmen, da die moderne Ernährung den Verzehr von verarbeiteten Pflanzenölen, Margarine und Transfetten anstelle ihrer natürlichen Alternativen wie Butter, Olivenöl, Avocado, Fischöl und Lebertran bevorzugt , fetter Fisch, Chiasamen usw. ...
Grundsätzlich essen wir zu viele Omega-6-Fettsäuren und zu wenig Omega-3-Fettsäuren. Die Lösung ist ganz einfach: Fangen Sie an, mehr Omega-3- und weniger Omega-6-Fettsäuren zu sich zu nehmen. Ihr allgemeiner Gesundheitszustand wird sich dramatisch verbessern und Ihr Stickoxidspiegel wird dabei ansteigen.
 Resveratrol ist ein Flavonoid aus der Gruppe der Polyphenole, das in Trauben und Rotwein vorkommt.
Resveratrol ist ein Flavonoid aus der Gruppe der Polyphenole, das in Trauben und Rotwein vorkommt.
Diese Verbindung wurde für mich interessant, als ich in mehreren Studien herausfand, dass sie den Testosteronspiegel erhöhen und den Östrogenspiegel senken kann, was genau das war, wonach ich gesucht hatte ...
Aber dann habe ich noch etwas anderes gefunden.
Resveratrol ist nicht nur gut für den Hormonhaushalt, es ist auch ein sehr starker Stickoxid-Booster, da es die Synthese des Enzyms Stickoxid stimuliert (Studie Nr. 1, Studie Nr. 2).
Um die Stickoxidproduktion auf natürliche Weise zu steigern, trinken Sie Rotwein, essen Sie Weintrauben und ergänzen Sie Ihre Ernährung möglicherweise mit einem Resveratrol-Nahrungsergänzungsmittel (das Nahrungsergänzungsmittel sollte Piperin enthalten, da Resveratrol selbst nicht sehr gut vom Körper aufgenommen wird)..
Abschluss
Jetzt haben Sie 20 Möglichkeiten, Ihren Stickoxidspiegel auf natürliche Weise zu erhöhen, zusammen mit einer kurzen Erklärung, was das bewirkt.
Denken Sie auch daran, dass Sie Ihre NO-Werte leicht überwachen können, indem Sie diese NO-Teststreifen zur Hand haben. Sie sind recht einfach zu bedienen und genau.
Danke an alle, die bis zum Ende gelesen haben!
Bei normalen Temperaturen ist N 2 O ein farbloses Gas mit einem schwach angenehmen Geruch und einem süßlichen Geschmack; hat eine narkotische Wirkung und verursacht zunächst krampfhaftes Lachen, dann Bewusstlosigkeit.
Methoden zur Beschaffung
1. Zersetzung von Ammoniumnitrat bei leichter Erwärmung:
NH 4 NO 3 = N 2 O + 2H 2 O
2. Wirkung von HNO 3 auf aktive Metalle
10HNO 3 (konz.) + 4Ca = N 2 O + 4Ca(NO 3) 2 + 5H 2 O
Chemische Eigenschaften
N 2 O weist weder saure noch basische Eigenschaften auf, d. h. es interagiert nicht mit Basen, Säuren oder Wasser (nicht salzbildendes Oxid).
Bei T > 500 „C zerfällt es in einfache Stoffe. N 2 O ist ein sehr starkes Oxidationsmittel. Beispielsweise ist es in der Lage, Schwefeldioxid in wässriger Lösung zu Schwefelsäure zu oxidieren:
N 2 O + SO 2 + H 2 O = N 2 + H 2 SO 4
NO – Stickoxid (II), Stickstoffmonoxid.
Bei normalen Temperaturen ist NO ein farb- und geruchloses Gas, schwer wasserlöslich und sehr giftig (in hohen Konzentrationen verändert es die Struktur des Hämoglobins).
Methoden zur Beschaffung
1. Direkte Synthese aus einfachen Substanzen kann nur bei sehr hohen T durchgeführt werden:
N 2 + O 2 = 2NO - Q
2. Produktion in der Industrie (1. Stufe der HNO 3 -Produktion).
4NH 3 + 5O 2 = 4NO + 6H 2 O
3. Labormethode – Verdünnungswirkung. HNO 3 für Schwermetalle:
8HNO 3 + 3Cu = 2NO + 3Cu(NO 3) 2 + 4H 2 O
Chemische Eigenschaften
NO ist ein nicht salzbildendes Oxid (wie N2O). Es hat Redox-Dualität.
I. NO – Oxidationsmittel
2NO + SO 2 + H 2 O = N 2 O + H 2 SO 4
2NO + 2H 2 = N 2 + 2H 2 O (mit Explosion)
II. NO – Reduktionsmittel
2NO + O 2 = 2NO 2
10NO + 6KMnO 4 + 9H 2 SO 4 = 10HNO 3 + 3K 2 SO 4 + 6MnSO 4 + 4H 2 O
NO 2 - Stickoxid (IV), Stickstoffdioxid
Bei normalen Temperaturen ist NO 2 ein rotbraunes giftiges Gas mit stechendem Geruch. Es ist eine Mischung aus NO 2 und seinem Dimer N 2 O 4 im Verhältnis -1:4. Stickstoffdioxid ist in Wasser gut löslich.
Methoden zur Beschaffung
I. Industriell - NO-Oxidation: 2NO + O 2 = 2NO 2
II. Labor:
Aktion der Konz. HNO 3 für Schwermetalle: 4HNO 3 + Cu = 2NO 2 + Cu(NO 3) 2 + 2H 2 O
Nitratzersetzung: 2Pb(NO 3) 2 = 4NO 2 + O 2 + 2PbO
Chemische Eigenschaften
NO 2 – Säureoxid, gemischtes Anhydrid aus 2 Säuren
NO 2 reagiert mit Wasser, basischen Oxiden und Alkalien. Die Reaktionen verlaufen jedoch nicht auf die gleiche Weise wie bei gewöhnlichen Oxiden – es handelt sich immer um Redoxreaktionen. Dies erklärt sich aus der Tatsache, dass CO keine Säure enthält. (N) = +4, daher disproportioniert NO 2, wenn es in Wasser gelöst wird, unter Bildung von 2 Säuren – Salpetersäure und Salpetersäure:
2NO 2 + H 2 O = HNO 3 + HNO 2
Erfolgt die Auflösung in Gegenwart von O 2, entsteht eine Säure – Salpetersäure:
4NO 2 + 2H 2 O + O 2 = 4HNO 3
Die Wechselwirkung von NO 2 mit Alkalien erfolgt auf ähnliche Weise:
in Abwesenheit von O 2: 2NO 2 + 2NaOH = NaNO 3 + NaNO 2 + H 2 O
in Gegenwart von O 2: 4NO 2 + 4NaOH + O 2 = 4NaNO 3 + 2H 2 O
NO 2 ist ein sehr starkes Oxidationsmittel
Hinsichtlich der Oxidationsfähigkeit ist NO 2 der Salpetersäure überlegen. In seiner Atmosphäre verbrennen C, S, P, Metalle und einige organische Substanzen. Dabei wird NO 2 zu freiem Stickstoff reduziert:
10NO 2 + 8P = 5N 2 + 4P 2 O 5
2NO 2 + 8HI = N 2 + 4I 2 + 4H 2 O (eine violette Flamme erscheint)
In Gegenwart von Pt oder Ni wird Stickstoffdioxid durch Wasserstoff zu Ammoniak reduziert:
2NO 2 + 7H 2 = 2NH 3 + 4H 2 O
NO 2 wird als Oxidationsmittel in Raketentreibstoffen verwendet. Bei der Wechselwirkung mit Hydrazin und seinen Derivaten wird eine große Energiemenge freigesetzt:
2NO 2 + 2N 2 H 4 = 3N 2 + 4H 2 O + Q
N 2 O 3 und N 2 O 5 sind instabile Substanzen
Beide Oxide haben einen ausgeprägt sauren Charakter und sind Anhydride der salpetrigen bzw. Salpetersäure.
N 2 O 3 liegt als Einzelstoff nur im festen Zustand unterhalb von T pl vor. (-10 0 C).
Mit steigender Temperatur zersetzt es sich: N 2 O 3 → NO + NO 2
N 2 O 5 zersetzt sich bei Raumtemperatur und insbesondere unter Licht so heftig, dass es manchmal spontan explodiert.
STICKOXID UND GESUNDHEIT
STICKOXID (NO) HAT VIELSEITIGE WIRKUNGEN IM KÖRPER.
Auf dieser Seite sind die verschiedenen Forschungsergebnisse zu den Auswirkungen von NO aufgeführt.
BLUTGEFÄSSE
NO reguliert die Erweiterung der Blutgefäße, d. h. Gefäßerweiterung. Stickstoffmonoxid spielt dabei eine entscheidende Rolle – es reguliert den systolischen Druck und die Blutgefäße. NO reguliert außerdem die glomeruläre und medulläre Blutversorgung und lindert Verspannungen im unteren Harntrakt. Mit Hilfe von NO werden im Körper neue Blutgefäße gebildet (Angiogenese). Mit Hilfe von NO funktioniert die verbesserte Durchblutung wie folgt:
heilt Wunden
stellt verlorene Sensibilität wieder her
hilft Schmerzen zu lindern
beschleunigt die Heilung von Frakturen
normalisiert den Blutdruck
verbessert die Blutversorgung der Kapillaren (Gewebeernährung)
verstärkt die Wirkung von Antibiotika
stärkt das Immunsystem (erhöht die Anzahl der T-Zellen)
CHOLESTERIN
Eine Erhöhung der Stickoxidmenge verringert die schädlichen Auswirkungen von Cholesterin. Ein Mangel an NO führt dazu, dass sich die Blutgefäße in Stresssituationen nicht erweitern. Das gleiche Phänomen wird bei Menschen beobachtet, die einen deutlich erhöhten Cholesterinspiegel haben.
ZENTRALES NERVENSYSTEM
Eine Erhöhung der Stickoxidmenge in den Zellen führt zu einer Verlängerung der Zelllebensdauer. Dies kann bei nicht-degenerativen Erkrankungen eingesetzt werden, bei denen Zellen vorzeitig absterben. Zu diesen Erkrankungen zählen die Parkinson-Krankheit und die Alzheimer-Krankheit.
TUMOREN UND KREBS
Antioxidantien schützen die Zellen. Wenn der antioxidative Schutz verloren geht, hängt das Zellleben von NO ab. Wenn NO die Zelle verlässt, stirbt die Zelle. Die Freisetzung von NO aus Zellen wird von pathogenen Zellen und Tumorzellen begrüßt. Wenn viel NO die Tumorzellen verlässt, zerstören Makrophagen die Tumorzellen. Von iNOS abgeleitetes Stickstoffmonoxid kann das Tumorwachstum beeinträchtigen. (Weiming
Stickstoffmonoxid kann Neoplasien und Magenkrebs hemmen. (Chinthalapally V. Rao, Nitric Oxide Signaling in Colon Cancer Chemoprevention, Mutation Research 2004 555: 107-119 Review).
KNOCHEN
Die Aktivität von Knochengewebezellen – Osteoblasten – stimuliert Stickoxid und erzeugt dadurch neues Knochengewebe. Andererseits beeinträchtigt NO die Aktivität von Osteoklasten, die Knochengewebe zerstören. NO sorgt für den Knochenstoffwechsel, so dass der Knochenaufbau schneller erfolgt als der Knochenabbau. Somit führt eine ausreichende Verfügbarkeit von Stickoxid zu einer schnellen Genesung.
Fröhlichkeit
Die Durchblutung und die Nervenimpulse erfolgen schnell. Die Zugabe kleiner Mengen NO verbessert die Vasodilatation (reguliert den Tonus der Blutgefäße) und erhöht die Empfindlichkeit (NO ist ein Neurotransmitter).
ALTER
NO und kein anderer Stoff kann die Alterung stoppen. Stickstoffmonoxid kann Blutgefäßthrombosen wirksam vorbeugen. Darüber hinaus beschleunigt NO die Wundheilung und Genesung nach einer Operation. Es liegen überzeugende Beweise dafür vor, dass NO die Leber schützt und das Immunsystem wirksam stärkt. All dies deutet darauf hin, dass NO einen Einfluss auf die Lebensverlängerung hat. Der Bedarf an Stickoxid steigt mit zunehmendem Alter, weil... Die körpereigene Produktion von NO nimmt ab.
METABOLISCHES SYNDROM
Der Diabetesforscher Gerald Raven gab 1988 einen allgemeinen Namen für Herzinfarkt-Risikofaktoren. Er versuchte zu zeigen, dass insbesondere bei Männern das Vorhandensein von Fleisch im Bauchbereich, ein niedriger HDL-Cholesterinspiegel, ein erhöhter Blutinsulinspiegel und ein hoher Blutdruck mit derselben Grunderkrankung verbunden sind. Dies wurde später als metabolisches Syndrom bekannt. Laut Reaven ist die Insulinresistenz der Hauptfaktor bei einem Herzinfarkt. Viele Studien deuten darauf hin, dass ein Mangel an Stickstoffmonoxid eine Ursache für Krankheiten wie Insulinresistenz, Diabetes bei Erwachsenen, Blutdruckprobleme und chronisches Müdigkeitssyndrom ist.
DRUCK
Hoher Blutdruck ist oft ein Signal dafür, dass der Stoffwechsel gestört ist, und oft ist der Hauptgrund dafür eine verminderte Stickoxidproduktion im Körper.
AIDS
Stickstoffmonoxid reduziert oder verhindert die Replikation des HIV-Virus (Torre D, Pugliese A, Speranza F., Role of nitric Oxide in HIV-1-Infektion: Freund oder Feind?, Lancet Infect Dis. 2003 Mar;3(3):128 -9; Antwort des Autors 129-30).
EREKTION
Unter dem Einfluss von Stickstoffmonoxid wird der Penis elastisch (A.L. Burnett et al, „Stickstoffoxid: ein physiologischer Mediator der Peniserektion“, Science, 17. Juli 1992).
Aktuelle Forschungsergebnisse zeigen, dass Stickstoffmonoxid ein die Erektion aufrechterhaltendes Gas ist (K. J. Hurt et al., „Alternatively spliced neuronal nitricoxide synthase mediates penile erection“, PNAS).
Da Stickstoff in seinen Verbindungen unterschiedliche Wertigkeiten aufweist, zeichnet sich dieses Element durch mehrere Oxide aus: Distickstoffoxid, Mono-, Tri-, Di- und Pentoxide des Stickstoffs. Schauen wir uns jeden von ihnen genauer an.
DEFINITION
Diastickstoffoxid(Lachgas, Lachgas) ist ein farbloses Gas, das thermisch stabil ist.
In Wasser schlecht löslich. Bei starker Abkühlung kristallisiert Klarwasser N 2 O×5,75H 2 O aus der Lösung.
DEFINITION
Stickstoffmonoxid Es kann entweder als farbloses Gas oder als blaue Flüssigkeit vorliegen.
Im festen Zustand ist es vollständig dimerisiert (N 2 O 2), im flüssigen Zustand – teilweise (≈ 25 % N 2 O 2), im Gas – in sehr geringem Maße. Extrem thermisch stabil. In Wasser schlecht löslich.
DEFINITION
Stickstofftrioxid ist eine thermisch instabile blaue Flüssigkeit.
Bei Raumtemperatur zerfällt es zu 90 % in NO und NO 2 und wird braun (NO 2), hat keinen Siedepunkt (NO verdampft zuerst). Im festen Zustand ist es eine weiße oder bläuliche Substanz mit ionischer Struktur – Nitrosylnitrit (NO +)(NO 2 –). In Gas hat es die molekulare Struktur ON-NO 2.
DEFINITION
Stickstoffdioxid(Fuchsschwanz) ist ein braunes Gas.
Bei Temperaturen über 135 °C handelt es sich um ein Monomer, bei Raumtemperatur um eine rotbraune Mischung aus NO 2 und seinem Dimer (Dianitrogentetroxid) N 2 O 4. Im flüssigen Zustand ist das Dimer farblos, im festen Zustand ist es weiß. Es löst sich gut in kaltem Wasser (eine gesättigte Lösung ist hellgrün) und reagiert vollständig damit.
DEFINITION
Stickstoffpentoxid (Salpetersäureanhydrid) ist ein weißer Feststoff, ein farbloses Gas und eine Flüssigkeit.
Beim Erhitzen sublimiert und schmilzt es; bei Raumtemperatur zersetzt es sich innerhalb von 10 Stunden. Im festen Zustand hat es eine ionische Struktur (NO 2 +)(NO 3 -) – Nitroylnitrat.
Tabelle 1. Physikalische Eigenschaften von Stickoxiden.
Gewinnung von Stickoxid
Unter Laborbedingungen wird Distickstoffoxid durch vorsichtiges Erhitzen von trockenem Ammoniumnitrat (1) oder durch Erhitzen einer Mischung aus Sulfaminsäure und Salpetersäure (73 %) (2) gewonnen:
NH 4 NO 3 = N 2 O + 2H 2 O (1);
NH 2 SO 2 OH + HNO 3 = N 2 O + H 2 SO 4 + H 2 O (2).
Stickstoffmonoxid entsteht durch die Wechselwirkung der einfachen Stoffe Stickstoff und Sauerstoff bei hohen Temperaturen (≈1300 o C):
N 2 + O 2 = 2NO.
Darüber hinaus ist Stickoxid (II) eines der Reaktionsprodukte der Auflösung von Kupfer in verdünnter Salpetersäure:
3Cu + 8HNO 3 = 3Cu(NO 3) 2 + 2NO + 4H 2 O.
Wenn ein Gasgemisch aus Stickoxiden (II) und (IV) auf -36 °C abgekühlt wird, entsteht Stickstofftrioxid:
NEIN + NEIN 2 = N 2 O 3.
Diese Verbindung kann durch Einwirkung von 50 %iger Salpetersäure auf Arsen(III)-oxid (3) oder Stärke (4) erhalten werden:
2HNO 3 + As 2 O 3 = NO 2 + NO + 2HAsO 3 (3);
HNO 3 + (C 6 H 10 O 5) n = 6nNO + 6nNO 2 + 6nCO 2 + 11nH 2 O (4).
Bei der thermischen Zersetzung von Blei(II)-nitrat entsteht Stickstoffdioxid:
2Pb(NO3)2 = 2PbO + 4NO2 + O2.
Die gleiche Verbindung entsteht, wenn Kupfer in konzentrierter Salpetersäure gelöst wird:
Cu + 4HNO 3 = Cu(NO 3) 2 + 2NO 2 + 2H 2 O.
Stickstoffpentoxid wird durch Überleiten von trockenem Chlor über trockenes Silbernitrat (5) sowie durch die Reaktion zwischen Stickoxid (IV) und Ozon (6) gewonnen:
2Cl 2 + 4AgNO 3 = 2N 2 O 5 + 4AgCl + O 2 (5);
2NO 2 + O 3 = N 2 O 5 + O 2 (6).
Chemische Eigenschaften von Stickoxid
Diastickstoffoxid ist leicht reaktiv und reagiert nicht mit verdünnten Säuren, Laugen, Ammoniakhydrat oder Sauerstoff. Beim Erhitzen reagiert es mit konzentrierter Schwefelsäure, Wasserstoff, Metallen und Ammoniak. Unterstützt die Verbrennung von Kohlenstoff und Phosphor. Bei der ORR kann es sowohl die Eigenschaften eines schwachen Oxidationsmittels als auch eines schwachen Reduktionsmittels aufweisen.
Stickstoffmonoxid reagiert nicht mit Wasser, verdünnten Säuren, Laugen oder Ammoniakhydrat. Fügt sofort Sauerstoff hinzu. Beim Erhitzen reagiert es mit Halogenen und anderen Nichtmetallen sowie starken Oxidations- und Reduktionsmitteln. Geht Komplexierungsreaktionen ein.
Stickstofftrioxid weist saure Eigenschaften auf und reagiert mit Wasser, Alkalien und Ammoniakhydrat. Reagiert heftig mit Sauerstoff und Ozon und oxidiert Metalle.
Stickstoffdioxid reagiert mit Wasser und Alkalien. Im OVR weist es die Eigenschaften eines starken Oxidationsmittels auf. Verursacht Korrosion von Metallen.
Stickstoffpentoxid weist saure Eigenschaften auf und reagiert mit Wasser, Alkalien und Ammoniakhydrat. Es ist ein sehr starkes Oxidationsmittel.
Anwendungen von Stickoxid
Distickstoffoxid wird in der Lebensmittelindustrie (ein Treibmittel bei der Herstellung von Schlagsahne), in der Medizin (zur Inhalationsanästhesie) und auch als Hauptbestandteil von Raketentreibstoff verwendet.
Stickstofftrioxid und -dioxid werden in der anorganischen Synthese zur Herstellung von Salpeter- und Schwefelsäure verwendet. Stickstoff(IV)-oxid wird auch als Bestandteil von Raketentreibstoff und gemischten Sprengstoffen verwendet.
Beispiele für Problemlösungen
BEISPIEL 1
| Übung | Stickoxid enthält 63,2 % Sauerstoff. Wie lautet die Formel des Oxids? |
| Lösung | Der Massenanteil des Elements X in einem Molekül der Zusammensetzung NX wird nach folgender Formel berechnet: ω (X) = n × Ar (X) / M (HX) × 100 %. Berechnen wir den Massenanteil von Stickstoff im Oxid: ω(N) = 100 % – ω(O) = 100 % – 63,2 % = 36,8 %. Bezeichnen wir die Anzahl der Mol der in der Verbindung enthaltenen Elemente mit „x“ (Stickstoff) und „y“ (Sauerstoff). Dann sieht das Molverhältnis wie folgt aus (die Werte der relativen Atommassen aus dem Periodensystem von D. I. Mendeleev sind auf ganze Zahlen gerundet): x:y = ω(N)/Ar(N) : ω(O)/Ar(O); x:y= 36,8/14: 63,2/16; x:y= 2,6: 3,95 = 1: 2. Dies bedeutet, dass die Formel für die Verbindung von Stickstoff und Sauerstoff NO 2 lautet. Das ist Stickstoffmonoxid (IV). |
| Antwort | NEIN 2 |
BEISPIEL 2
| Übung | Welche Gase sind schwerer und welche um wie viel leichter als Luft: Kohlendioxid, Stickstoffdioxid, Kohlenmonoxid, Chlor, Ammoniak? |
| Lösung | Das Verhältnis der Masse eines gegebenen Gases zur Masse eines anderen Gases im gleichen Volumen, bei gleicher Temperatur und gleichem Druck wird als relative Dichte des ersten Gases zum zweiten bezeichnet. Dieser Wert gibt an, wie oft das erste Gas schwerer oder leichter ist als das zweite Gas. Das relative Molekulargewicht der Luft wird mit 29 angenommen (unter Berücksichtigung des Gehalts an Stickstoff, Sauerstoff und anderen Gasen in der Luft). Es ist zu beachten, dass der Begriff „relative Molekülmasse der Luft“ bedingt verwendet wird, da Luft ein Gasgemisch ist. D Luft (CO 2) = M r (CO 2) / M r (Luft); D Luft (CO 2) = 44 / 29 = 1,52. M r (CO 2) = A r (C) + 2 × A r (O) = 12 + 2 × 16 = 12 + 32 = 44. D Luft (NO 2) = M r (NO 2) / M r (Luft); D Luft (NO 2) = 46 / 29 = 1,59. M r (NO 2) = A r (N) + 2 × A r (O) = 14 + 2 × 16 = 14 + 32 = 46. D Luft (CO) = M r (CO) / M r (Luft); D Luft (CO) = 28 / 29 = 0,97. M r (CO) = A r (C) + A r (O) = 12 + 16 = 28. D Luft (Cl 2) = M r (Cl 2) / M r (Luft); D Luft (Cl 2) = 71 / 29 = 2,45. M r (Cl 2) = 2 × A r (Cl) = 2 × 35,5 = 71. D Luft (NH 3) = M r (NH 3) / M r (Luft); D Luft (NH 3) = 17 / 29 = 0,57. M r (NH 3) = A r (N) + 3 ×A r (H) = 14 + 3 ×1 = 17. |
| Antwort | Kohlendioxid, Stickstoffdioxid und Chlor sind jeweils 1,52 schwerer als Luft; 1,59- bzw. 2,45-fach, Kohlenmonoxid und Ammoniak sind 0,97- bzw. 0,57-fach leichter. |