ทะเลสาบน้ำแข็งขนาดใหญ่บนดาวอังคารและแผนของ Musk - yuri_egorow — LiveJournal ปฏิกิริยาที่กำหนดของนักเคมีในการแก้ปัญหาชิ้นส่วนด้วยเครื่องปฏิกรณ์ Sabatier
นักเคมีชาวฝรั่งเศส Paul Sabatier เกิดที่เมืองการ์กาซอนทางตอนใต้ของฝรั่งเศส พ่อแม่ของเขาคือ Pauline (Gilam) Sabatier และ Alexis Sabatier เจ้าของที่ดินซึ่งสูญเสียทรัพย์สินเนื่องจากการไม่ชำระหนี้จึงเปิดร้านขายหมวก เอส เป็นหนึ่งในลูกชายสามคนและเป็นลูกคนเล็กในครอบครัวที่มีลูกเจ็ดคน เด็กชายที่มีความอยากรู้อยากเห็นและชาญฉลาดเรียนที่ Lyceum ในเมือง Carcassonne ซึ่งครูถือว่าเขาเป็นนักเรียนที่มีความสามารถและขยัน เอสเองมักพูดว่า: “ฉันเรียนวิชาที่ฉันชอบน้อยที่สุดเป็นส่วนใหญ่” ในปี พ.ศ. 2411 เขาย้ายไปที่ Toulouse Lyceum เพื่อเตรียมตัวสอบเข้ามหาวิทยาลัย ในเมืองตูลูส S. ยังเข้าร่วมการบรรยายสาธารณะเกี่ยวกับฟิสิกส์และเคมี ซึ่งเป็นครั้งแรกที่ปลุกความปรารถนาในตัวเขาให้มีส่วนร่วมในการวิจัยทางวิทยาศาสตร์
ก่อนที่จะไปปารีสเพื่อฝึกฝนเพิ่มเติมอีกสองปี ส. ในปี พ.ศ. 2412...2415 ศึกษาภาษาและวรรณคดีคลาสสิกที่เซนต์ แมรี่ในตูลูส ในปี พ.ศ. 2417 เขาได้อันดับหนึ่งในการสอบเข้าและได้รับการยอมรับทั้งใน École Normale Superior และ École Polytechnique เมื่อเลือกอย่างหลัง S. สำเร็จการศึกษาในสามปีและเป็นนักเรียนที่ดีที่สุดในกลุ่ม ในปีต่อมาเขาสอนฟิสิกส์ที่ Lycée ในเมืองนีมส์ จากนั้นก็ได้เป็นผู้ช่วยของนักเคมี Marcelin Berthelot ที่ Collège de France ที่นี่ S. เรียนต่อและในปี พ.ศ. 2423 ได้รับปริญญาเอกสาขาวิทยานิพนธ์เกี่ยวกับอุณหเคมีของกำมะถันและโลหะซัลเฟต
ในปีหน้า S. ศึกษาฟิสิกส์ที่มหาวิทยาลัยบอร์กโดซ์ เมื่อกลับมาที่ตูลูสในปี พ.ศ. 2425 สองปีต่อมาเขาได้รับตำแหน่งประธานสาขาเคมีที่มหาวิทยาลัยตูลูสซึ่งเขาเป็นหัวหน้าจนกระทั่งสิ้นสุดอาชีพทางวิทยาศาสตร์ของเขา ในปี 1905 S. ได้รับการแต่งตั้งเป็นคณบดีคณะ และแม้ว่าในปี 1907 เขาได้รับคำเชิญให้เข้ารับตำแหน่งของ Henri Moissan ที่มหาวิทยาลัยปารีส (Sorbonne) เขาก็เลือกที่จะอยู่ในตูลูส
เช่นเดียวกับ Berthelot, S. ในช่วงเริ่มต้นของกิจกรรมการวิจัยของเขามุ่งเน้นไปที่ปัญหาเคมีอนินทรีย์ โดยใช้วิธีการกลั่นสุญญากาศ เขาได้ไฮโดรเจนไดซัลไฟด์บริสุทธิ์ นักวิทยาศาสตร์ยังแยกส่วนประกอบไบนารีของโบรอนและซิลิคอน ค้นพบโลหะไนไตรด์ใหม่ๆ หลายชนิด และพัฒนาวิธีการเตรียมกรดไนโตรซิล ไดซัลเฟอร์ และเกลือทองแดง-เงินผสมพื้นฐาน
ในช่วงทศวรรษที่ 1890 ส.หันมาเรียนเคมีอินทรีย์ เขาเริ่มสนใจเป็นพิเศษในกระบวนการเร่งปฏิกิริยาที่เกี่ยวข้องกับไฮโดรจิเนชัน ซึ่งทำให้สารประกอบอินทรีย์ที่ไม่อิ่มตัวอิ่มตัว (สารประกอบไม่อิ่มตัวสามารถเติมสารเคมีได้ ในขณะที่สารประกอบอิ่มตัวไม่แสดงแนวโน้มเช่นนี้) ในเวลาเดียวกัน ตัวเร่งปฏิกิริยาในปฏิกิริยาดังกล่าวมักจะเป็นแพลทินัมและแพลเลเดียม และต้นทุนที่สูงทำให้ไม่สามารถนำไปใช้ในอุตสาหกรรมขนาดใหญ่ได้ S. เป็นที่รู้จักจากการทดลองซึ่งได้รับนิกเกิลคาร์บอนิลโดยการเปิดเผยนิกเกิลที่ถูกบดกับการกระทำของคาร์บอนมอนอกไซด์ เมื่อรู้ว่าปฏิกิริยาที่คล้ายกันนี้เกิดขึ้นเมื่อนำเหล็กมาแทนนิกเกิล S. จึงสงสัยว่าเป็นไปได้หรือไม่ที่จะทำให้ก๊าซอื่นทำปฏิกิริยากับนิกเกิลและโลหะอื่นๆ ในปี พ.ศ. 2439 เขาได้รับไนโตรเจนเปอร์ออกไซด์โดยมีทองแดง โคบอลต์ และนิกเกิล
เมื่อ S. ทราบว่า Moissan และ Charles Moreau นักเคมีชาวฝรั่งเศสอีกคน ล้มเหลวในการบรรลุผลเดียวกันโดยใช้อะเซทิลีน S. ได้ทำการทดลองซ้ำ โดยนำเอทิลีนซึ่งเป็นสารที่มีปฏิกิริยาน้อยกว่ามาก และส่งก๊าซเอทิลีนไปเหนือเงินและนิกเกิล เขาสังเกตเห็นว่าที่อุณหภูมิ 300°C อุณหภูมิที่เพิ่มขึ้นจะเรืองแสง คาร์บอนจะสะสมอยู่บนนิกเกิล และก๊าซจะถูกปล่อยออกมา จากข้อมูลของ Moissan และ Moreau ก๊าซนี้ควรเป็นไฮโดรเจน S. ค้นพบว่าก๊าซประกอบด้วยอีเทนเป็นส่วนใหญ่ ซึ่งเป็นสารประกอบที่อิ่มตัวด้วยไฮโดรเจน แทนที่จะจับเอทิลีน นิกเกิลที่บดแล้วจะถูกใช้เป็นตัวเร่งปฏิกิริยาในการผลิตสารประกอบคาร์บอนที่เติมไฮโดรเจน
เนื่องจากไฮโดรคาร์บอนอิ่มตัวเป็นตัวกลางที่สำคัญในการผลิตยา น้ำหอม ผงซักฟอก ไขมันที่บริโภคได้ และผลิตภัณฑ์อุตสาหกรรมอื่นๆ การค้นพบโดย S. จึงมีคุณค่าในทางปฏิบัติอย่างมาก อย่างไรก็ตาม นักวิทยาศาสตร์ได้รับสิทธิบัตรเพียงไม่กี่ฉบับสำหรับการค้นพบของเขา แม้ว่าเขาจะยังคงมีส่วนร่วมในการวิจัยทางวิทยาศาสตร์ต่อไปก็ตาม ทำงานร่วมกับนักเรียนของเขา Zh.B. แซนเดอรันเขาได้พิสูจน์ความสามารถของนิกเกิลในการเติมไฮโดรเจน (ไฮโดรเจน) ไฮโดรคาร์บอนอื่นๆ
ในปี 1912 S. ได้รับรางวัลโนเบลสาขาเคมี "สำหรับวิธีการเติมไฮโดรเจนของสารประกอบอินทรีย์ที่เสนอโดยมีโลหะละเอียด ซึ่งกระตุ้นการพัฒนาเคมีอินทรีย์ได้อย่างมาก" S. แบ่งปันรางวัลนี้กับนักเคมีชาวฝรั่งเศส Victor Grignard “ตลอด 15 ปีที่ผ่านมา” เอส. กล่าวในการบรรยายโนเบล “ความคิดเกี่ยวกับกลไกของการเร่งปฏิกิริยาไม่เคยละทิ้งผมเลย ความสำเร็จทั้งหมดของฉันเป็นผลมาจากข้อสรุปที่เธอสร้างขึ้น” “ทฤษฎีไม่สามารถเรียกร้องความเป็นอมตะได้” เขากล่าวเสริม “นี่เป็นเพียงคันไถที่คนไถใช้ไถพรวน ซึ่งเขามีสิทธิ์ทุกประการที่จะเปลี่ยนคันไถให้สมบูรณ์ยิ่งขึ้นหลังเก็บเกี่ยว”
หนึ่งปีหลังจากได้รับรางวัลโนเบล นักวิทยาศาสตร์ได้ตีพิมพ์การค้นพบของเขา (เขารวบรวมพวกมันไว้ในเอกสารทั่วไปเรื่อง "การเร่งปฏิกิริยาในเคมีอินทรีย์" ซึ่งแปลเป็นหลายภาษารวมถึงภาษารัสเซียด้วย - เอ็ด) แนวคิดของ S. ขัดแย้งกับทฤษฎีที่เสนอโดย Wilhelm Ostwald ก่อนหน้านี้ Ostwald เชื่อว่ารีเอเจนต์ที่เป็นก๊าซซึ่งชนกับตัวเร่งปฏิกิริยาที่เป็นของแข็งจะถูกดูดซับโดยไมโครพอร์ S. แนะนำว่าปฏิกิริยาดังกล่าวเกิดขึ้นที่พื้นผิวด้านนอกของตัวเร่งปฏิกิริยา ซึ่งนำไปสู่การก่อตัวของสารประกอบกลางชั่วคราวที่ไม่เสถียร จากนั้นสารประกอบที่ไม่เสถียรจะถูกย่อยสลายเพื่อสร้างผลิตภัณฑ์ขั้นสุดท้าย โดยสังเกตผลผลิตที่ได้ แนวคิดทั่วไปนี้ยังคงใช้ได้เมื่อประเมินประสิทธิภาพของตัวเร่งปฏิกิริยาที่เพิ่งค้นพบ
ในปีพ. ศ. 2472 เอส. ลาออกจากตำแหน่งคณบดีคณะที่มหาวิทยาลัยตูลูสและในปีถัดมาเขาก็ลาออก
ในปี พ.ศ. 2427 S. ได้รวมชะตากรรมของเขากับ Germaine Eral ลูกสาวของผู้พิพากษาท้องถิ่น พวกเขามีลูกสาวสี่คน หลังจากภรรยาของเขาเสียชีวิตในปี พ.ศ. 2441 เอสก็ไม่เคยแต่งงานอีกเลย จนกระทั่งปี 1939 เมื่อสุขภาพของเขาเริ่มแย่ลง นักวิทยาศาสตร์ยังคงบรรยายต่อที่มหาวิทยาลัยตูลูส เป็นคนใจเย็นเอาแต่ใจตัวเอง ส. เสียชีวิตเมื่อวันที่ 14 สิงหาคม พ.ศ. 2484 ในเมืองตูลูส
นอกจากรางวัลโนเบลแล้ว S. ยังได้รับรางวัล Jacker Prize จาก French Academy of Sciences (1905), Davy Medal (1915) และ Royal Medal (1918) ของ Royal Society of London รวมถึง Franklin Medal of สถาบันแฟรงคลิน (1933) S. ได้รับปริญญากิตติมศักดิ์จากมหาวิทยาลัยเพนซิลเวเนียและซาราโกซา เขาเป็นสมาชิกของ French Academy of Sciences และเป็นสมาชิกชาวต่างชาติของสมาคมวิทยาศาสตร์หลายแห่ง รวมถึง Royal Society of London, Madrid Academy of Sciences สถาบันวิทยาศาสตร์แห่งเนเธอร์แลนด์, สมาคมเคมีอเมริกัน, สมาคมวิทยาศาสตร์แห่งบรัสเซลส์ และสมาคมเคมีแห่งอังกฤษ
ตามวิกิพีเดีย:
ปฏิกิริยาซาบาเทียร์เกี่ยวข้องกับปฏิกิริยาของไฮโดรเจนกับคาร์บอนไดออกไซด์ที่อุณหภูมิสูงขึ้น (อุณหภูมิที่เหมาะสมที่สุด 300-400 °C) และความดันเมื่อมีตัวเร่งปฏิกิริยานิกเกิลเพื่อผลิตมีเทนและน้ำ $$ CO_2 + 4H_2 \ ลูกศรขวา CH_4 + H_2O + \ ข้อความ (พลังงาน) $$
ดังที่คุณเห็นจากปฏิกิริยาเคมีก่อนหน้านี้ ในการที่จะได้ 1 KMole CH_4 คุณต้องมีไฮโดรเจน 4 Kmole เป็นสารตั้งต้นและมีตัวกลางในการทำปฏิกิริยาที่ 300-400 °C (พระเจ้ารู้ว่าคุณต้องการตัวเร่งปฏิกิริยามากแค่ไหน)
เมื่อเปรียบเทียบกับเครื่องยนต์สันดาปมีเทนทั่วไป:
- ไฮโดรเจนไม่มีอยู่ในอากาศโดยรอบถึงระดับที่ทำให้เกิดปฏิกิริยาซาบาเทียร์ได้อย่างยั่งยืน (ไม่ใช่ออกซิเจน) ซึ่งหมายความว่าคุณต้องมีถังแยกสำหรับไฮโดรเจนพร้อมกับเครื่องยนต์ของคุณ (ไม่ต้องพูดถึงลักษณะการระเบิดของไฮโดรเจน)
- การอุ่นสารตั้งต้นไว้ที่ 300-400 °C จะต้องมีการเผาไหม้ภายนอก หากดำเนินการโดยใช้เชื้อเพลิงไฮโดรคาร์บอน ซึ่งจะต้องมีห้องเผาไหม้และเครื่องแลกเปลี่ยนความร้อนเพิ่มเติม
- ค่าความร้อนที่สูงขึ้นของมีเทน = 889 kJ/mol และ HHV ของไฮโดรเจน = 286 kJ/mol (Wikipedia) ดังนั้นในทางทฤษฎีแล้ว ปฏิกิริยา Sabatier จะให้ CH4 1 โมล โดยมีค่าความร้อน 889 kJ ป้อนให้กับเครื่องปฏิกรณ์ 4 โมลของ H2 ซึ่ง มีค่าความร้อน 4* 286 = 1144 kJ!!
- มีเทนและน้ำที่ได้จะมีอัตราส่วน 1:1 การแนะนำส่วนผสมนี้กับน้ำปริมาณเท่านี้ก่อนเข้าสู่ห้องเผาไหม้จะทำให้คุณมีกระบวนการเผาไหม้ที่มีประสิทธิภาพต่ำมาก ดังนั้นโดยธรรมชาติแล้ว คุณจะต้องมีกลไกการแยกเพื่อลดปริมาณน้ำได้มากเท่ากับ เป็นไปได้ก่อนเข้าห้องเผาไหม้
มีใครค้นคว้า/สร้างรถยนต์ที่เผาไหม้มีเทนและนำมันกลับมา (อย่างน้อยบางส่วน) จากไอเสียผ่านปฏิกิริยา Sabatier หรือไม่?
ฉันไม่รู้จริงๆ แต่จากประเด็นก่อนหน้านี้ ฉันไม่เห็นว่าสิ่งนี้จะเกิดขึ้นได้เลยกับเครื่องยนต์สันดาปภายในแบบธรรมดาที่ใช้มีเทน
Algo ให้คำตอบที่ดีเกี่ยวกับรายละเอียดแก่คุณ มีคำตอบที่กว้างกว่าและใช้กันอย่างแพร่หลายมากขึ้น
การแปลงพลังงานรูปแบบใดก็ตามให้เป็นความร้อนจะทำให้เกิดความไร้ประสิทธิภาพอย่างมาก นี่เป็นพลังงานรูปแบบคุณภาพต่ำ ดังนั้นหากคุณต้องการทำงานกับพลังงานนี้เลย ทางที่ดีควรทำก่อนที่มันจะกลายเป็นความร้อน ทุกครั้งที่เป็นไปได้
เมื่ออยู่ในรูปของความร้อนคุณภาพของพลังงาน (ที่เราเรียกว่า ออกกำลังกายนั่นคือความสามารถในการทำงาน) ขึ้นอยู่กับความแตกต่างระหว่างอุณหภูมิกับอุณหภูมิเย็นของถังที่คุณใช้เป็นหม้อน้ำ โดยปกติจะเป็นอุณหภูมิแวดล้อมแต่ไม่เสมอไป หากคุณต้องการทำงานใดๆ กับความร้อนนี้ ให้ทำเมื่ออุณหภูมิต่างกันสูงสุดและอุณหภูมิอ่างเก็บความเย็นต่ำสุด
ดังนั้นคุณจึงไม่เปลี่ยนจากความร้อนไปเป็นพลังงานเคมีเป็นพลังงานจลน์
เมื่อใดก็ตามที่คุณทำการเปลี่ยนแปลงพลังงาน คุณจะสูญเสียความสามารถในการทำงาน กล่าวคือ คุณจะสูญเสียการออกกำลังกายบางประเภท เมื่อคุณไม่ร้อนเพื่อแปลงความร้อน คุณจะสูญเสีย มากออกกำลังกาย ดังนั้นกระบวนการกลับไปกลับมา เช่น พลังงานเคมี (มีเทน) เพื่อให้ความร้อนแล้วกลับมาอีกครั้ง นั้นไม่มีประสิทธิภาพเลย และคุณจะได้กลับมาน้อยกว่าที่คุณได้รับมาก
ไม่เลย คุณจะไม่ใช้กระบวนการ Sabatier เพื่อควบคุมยานพาหนะเพราะมันจะเกี่ยวข้องกับ:
พลังงานเคมี --> ความร้อน -->
พลังงานเคมี --> ความร้อน --> พลังงานจลน์
และไม่สำคัญว่ากระบวนการแปลงจะเป็นอย่างไรในฟิลด์นี้ ซึ่งปัจจุบันมีป้ายกำกับว่า "Sabatier": ชุดของ Conversion ที่สับสนนี้ไม่สมเหตุสมผล ไม่ว่ากระบวนการนั้นจะเป็นอย่างไรก็ตาม
แต่คุณเพียงแค่เปลี่ยนจากพลังงานเคมีไปสู่ความร้อนเป็นพลังงานจลน์ ซึ่งเป็นสิ่งที่เครื่องยนต์สันดาปภายในทำ
การเปลี่ยนจากมีเธนเป็นความร้อนเป็นมีเทนจะไม่ได้ผลมากนัก คุณจะทำเฉพาะในสถานการณ์ที่พิเศษจริงๆ เท่านั้นตอนนี้ฉันคิดไม่ออก แต่ฉันแน่ใจว่ามีคนสามารถประดิษฐ์กรณีมุมที่สมเหตุสมผลได้ เช่น. มีเหตุการณ์แปลกประหลาดบางประการที่คุณสามารถเคลื่อนย้ายความร้อนคุณภาพสูงได้แต่ไม่สามารถเคลื่อนย้ายมีเทนได้
ดังนั้นจึงไม่มีประโยชน์ที่จะนำกระบวนการ Sabatier (หรือที่คล้ายกัน) มาใช้กับรถยนต์มีเทน หากคุณต้องการประสิทธิภาพที่สูงขึ้น คุณต้องลงทุนในประสิทธิภาพของยานพาหนะ: ความเร็วต่ำลง เครื่องยนต์ที่มีอุณหภูมิสูงขึ้น สะอาดขึ้น น้ำหนักรถเบาขึ้น โปรไฟล์ตามหลักอากาศพลศาสตร์มากขึ้น ระบบส่งกำลังที่มีประสิทธิภาพสูง ระบบนำพลังงานจลน์กลับมาใช้ใหม่ ฯลฯ สิ่งที่คุณ ไม่ปฏิบัติตามคือการเพิ่มน้ำหนักโดยการเพิ่มชุดอุปกรณ์ที่ไม่จำเป็นที่ไม่มีประสิทธิภาพเพื่อเปลี่ยนความร้อนของคุณกลับเป็นเชื้อเพลิง: เพียงแค่เผาผลาญเชื้อเพลิงน้อยลง
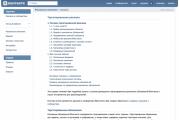
แผนการตั้งอาณานิคมบนดาวอังคารมักถือว่าการเข้าถึงน้ำค่อนข้างง่าย พบทะเลสาบขนาดใหญ่ (น้ำแข็ง 14,300 ลูกบาศก์กิโลเมตร) - แผนที่ในภาพ - สอดคล้องกับแผนอย่างสมบูรณ์
มาจำแผนของ Musk กัน โดยฉันอ้างอิงคำต่อคำ ตามด้วยการแปล ความคิดเห็น และรายละเอียดจากสุนทรพจน์อื่นๆ ของ Elon
1.
ส่งภารกิจสอดแนมมังกร ในตอนแรกเพียงเพื่อให้แน่ใจว่าเรารู้วิธีลงจอดโดยไม่ต้องเพิ่มปล่องภูเขาไฟ จากนั้นจึงหาวิธีที่ดีที่สุดในการรับน้ำสำหรับปฏิกิริยา CH4/O2 Sabatier
2.
ยานอวกาศ Heart of Gold บินไปยังดาวอังคารซึ่งเต็มไปด้วยอุปกรณ์สำหรับสร้างจรวดขับเคลื่อนเท่านั้น
3.
ภารกิจแรกที่มีลูกเรือพร้อมอุปกรณ์เพื่อสร้างฐานพื้นฐานและสร้างโรงงานผลิตจรวดให้เสร็จสมบูรณ์
4.
พยายามเพิ่มจำนวนเที่ยวบินเป็นสองเท่าในแต่ละการพบกันในวงโคจรโลก-ดาวอังคาร ซึ่งก็คือทุกๆ 26 เดือน จนกว่าเมืองจะเติบโตได้ด้วยตัวเอง
ข้อความของมันคือ ตัวเอียงความคิดเห็นของฉันตรงไปตรงมา
1. ส่งมังกรไปสอบสวน ขั้นแรกเพื่อให้แน่ใจว่าเรารู้วิธีที่จะลงจอดเรือโดยไม่ต้องเพิ่มปล่องภูเขาไฟอีก และจากนั้นก็หาวิธีที่ดีที่สุดในการผลิตน้ำสำหรับปฏิกิริยา CH4/O2 Sabatier
อย่าเพิ่มปล่องภูเขาไฟ
อีลอนพูดติดตลกว่าการเพิ่มปล่องภูเขาไฟหมายถึงการทำลายยานลงจอด การพูดคุยของเขาเกิดขึ้นหลังจากภารกิจ Exo Mars เพิ่มปล่องภูเขาไฟที่สวยงามบนพื้นผิวโลก Dragon คือภารกิจ Red Dragon ซึ่งมีกำหนดเปิดตัวในปี 2561 ซึ่งหมายถึงการทดสอบและสาธิตการลงจอดในแนวดิ่งบนเครื่องยนต์ คล้ายกับการลงจอดบนคอสโมโดรมและแพลตฟอร์มลอยน้ำ “แน่นอน ฉันยังรักคุณอยู่”
ภารกิจมังกรแดง
มังกรจะเต็มไปด้วยหุ่นยนต์สำหรับการสำรวจและการขุด เห็นได้ชัดว่า SpaceX จะสั่งหุ่นยนต์จากองค์กรอื่น แต่การตัดสินใจครั้งนี้ยังไม่ได้ประกาศ Musk ยังมีบริษัทหุ่นยนต์ของตัวเอง โดยเขาได้ลงทุนไปแล้วอย่างน้อยหนึ่งพันล้านดอลลาร์
ปฏิกิริยาของน้ำและซาบาเทียร์
ปฏิกิริยาเคมีสองรายการและการติดตั้งปฏิกิริยาเคมีสองรายการจะเป็นองค์ประกอบหลักในระยะเริ่มแรกของการล่าอาณานิคม: ปฏิกิริยาอิเล็กโทรไลซิสของน้ำ b. ปฏิกิริยาซาบาเทียร์
ก. 2H2O = 2H2 + O2 - ในปฏิกิริยานี้ การสลายตัวของน้ำจะผลิตออกซิเจนและไฮโดรเจน
ข. CO2 + 4H2 → CH4 + 2H2O + พลังงาน - เมื่อทำปฏิกิริยากับคาร์บอนไดออกไซด์ในชั้นบรรยากาศดาวอังคาร ไฮโดรเจนจะผลิตมีเทนและน้ำ ปฏิกิริยาซาบาเทียร์จะปล่อยพลังงานออกมาซึ่งสามารถ/ควรใช้ได้
มีเทนและออกซิเจนเป็นเชื้อเพลิงและออกซิไดเซอร์สำหรับเรือซีรีส์ ITS (Interplanetary Transport Ship) ซึ่งลำแรกจะได้รับชื่ออันเป็นเอกลักษณ์ว่า "Heart of Gold"
สิ่งที่น่าสนใจคือศูนย์ปฏิกิริยาซาบาเทียร์ได้ถูกสร้างขึ้นและทดสอบที่ความเข้มข้นของคาร์บอนไดออกไซด์ที่สอดคล้องกับบรรยากาศของดาวอังคาร แต่สิ่งนี้จะพัฒนาและปรับปรุง
2. The Heart of Gold จะบินไปยังดาวอังคาร โดยเต็มไปด้วยอุปกรณ์ที่จำเป็นในการสร้างโรงงานผลิตเชื้อเพลิงเท่านั้น
"หัวใจสีทอง" จะบินในโหมดไร้คนขับและทิ้งอุปกรณ์และวัสดุน้ำหนักมากถึง 100 ตันลงบนพื้นผิวดาวอังคาร โดยพื้นฐานแล้ว นี่จะเป็นอุปกรณ์ที่จำเป็นสำหรับการดำเนินการในระดับอุตสาหกรรมในการสกัดน้ำและการผลิตปฏิกิริยา 2 อย่างนี้: อิเล็กโทรไลซิสของน้ำและซาบาเทียร์ แน่นอนว่าอุปกรณ์นี้รวมแหล่งพลังงานไว้ด้วย
3. เป้าหมายของภารกิจบรรจุมนุษย์ชุดแรกคือการสร้างฐานที่มีสิ่งจำเป็นและสร้างโรงงานผลิตเชื้อเพลิงให้เสร็จสมบูรณ์
ภารกิจบรรจุมนุษย์ครั้งแรกจะมี 12 คน Elon มีแนวคิดเฉพาะเจาะจงมากมายเกี่ยวกับสิ่งที่ "ฐานที่มีสิ่งจำเป็น" ควรประกอบด้วย - ชื่อคือ Mars Base Alpha - แต่ตอนนี้ไม่ใช่เวลาที่จะหารือในรายละเอียดทั้งหมด มีการวางแผนที่จะใช้อุโมงค์และถ้ำธรรมชาติที่ NASA ค้นพบแล้ว และการก่อสร้างสถานที่ใต้ดินอื่นๆ บนพื้นผิว เต็นท์โปร่งใสทำจากแก้วและเสริมด้วยคาร์บอนไฟเบอร์
เห็นได้ชัดว่างานหลักคือความสมบูรณ์ของการก่อตั้งวิสาหกิจอุปกรณ์ที่ Golden Heart จะจัดหา: การผลิตน้ำ, พลังงาน, ปฏิกิริยาอิเล็กโทรไลซิส, ปฏิกิริยาซาบาเทียร์
4. หลังจากนั้น ภารกิจจะเป็นการเพิ่มจำนวนเรือเป็นสองเท่าในการเผชิญหน้าโลก-ดาวอังคารแต่ละครั้ง ซึ่งจะเกิดขึ้นทุกๆ 26 เดือน จนกว่าเมืองจะเริ่มเติบโตอย่างเป็นอิสระ
ไม่มีอะไรจะแสดงความคิดเห็นที่นี่ มีปัญหาที่แก้ไม่ได้หลายร้อยข้อ แม้ว่ามีเพียงสองข้อเท่านั้นที่ดูยาก: กฎของการมีปฏิสัมพันธ์กับชีวมณฑลพื้นเมืองของดาวอังคาร (ซึ่งอาจมีอยู่และอาจเปราะบางมาก) และดูว่าทารกจะตั้งครรภ์ตามปกติและเกิดที่ 1/3 ของแรงโน้มถ่วงของโลกหรือไม่
ทะเลสาบน้ำแข็งตั้งอยู่ในพื้นที่ที่สะดวกของดาวอังคาร ละติจูดกลาง มีที่ราบมากหลายแห่งที่เหมาะสำหรับลงจอด ชั้นดินที่ปกคลุมน้ำแข็งมีความหนาตั้งแต่หนึ่งถึงสิบเมตร น้ำแข็งยังผสมกับทรายบางส่วน แต่ความบริสุทธิ์ของน้ำแข็งอยู่ภายใน 50-85% ความลึกของทะเลสาบน้ำแข็งอยู่ระหว่าง 100 ถึง 200 เมตร
ปริมาณน้ำสำรองเทียบได้กับหนึ่งใน American Great Lakes - "Superior"
ในฐานะที่เป็นตัวเร่งปฏิกิริยาที่มีประสิทธิภาพมากขึ้น สามารถใช้รูทีเนียมกับอะลูมิเนียมออกไซด์ได้ กระบวนการนี้อธิบายได้ด้วยปฏิกิริยาต่อไปนี้:
CO 2 + 4H 2 → CH 4 + 2H 2 O
การช่วยชีวิตสถานีอวกาศ
ปัจจุบัน เครื่องกำเนิดออกซิเจนบนสถานีอวกาศนานาชาติผลิตออกซิเจนจากน้ำผ่านกระบวนการอิเล็กโทรลิซิส และปล่อยไฮโดรเจนที่เกิดขึ้นออกสู่อวกาศ ออกซิเจนที่หายใจเข้าไปจะก่อให้เกิดคาร์บอนไดออกไซด์ ซึ่งจะต้องกำจัดออกจากอากาศและกำจัดทิ้งในภายหลัง แนวทางนี้ต้องใช้น้ำปริมาณมากในการจ่ายให้กับสถานีอวกาศเป็นประจำเพื่อผลิตออกซิเจน นอกเหนือจากน้ำสำหรับดื่ม สุขอนามัย ฯลฯ น้ำปริมาณมากนี้จะไม่สามารถใช้ได้กับภารกิจระยะยาวนอกวงโคจรโลกในอนาคต
วิธีแก้ปัญหาที่สามและอาจดีกว่าสำหรับปัญหาปริมาณสัมพันธ์คือการรวมปฏิกิริยาซาบาเทียร์และปฏิกิริยาของไฮโดรเจนกับคาร์บอนไดออกไซด์ในเครื่องปฏิกรณ์เดี่ยวดังต่อไปนี้:
3CO 2 + 6H 2 → CH 4 + 2CO + 4H 2 O
ปฏิกิริยานี้เป็นปฏิกิริยาคายความร้อนเล็กน้อย และเมื่อทำปฏิกิริยากับน้ำด้วยไฟฟ้า จะทำให้ได้อัตราส่วนระหว่างออกซิเจนและมีเทนที่ 4:1 ทำให้มีออกซิเจนสำรองจำนวนมาก ตามโครงการนี้ เมื่อมีเพียงไฮโดรเจนเบาเท่านั้นถูกส่งมาจากโลก และมีออกซิเจนหนักและคาร์บอนถูกผลิตขึ้นที่ไซต์งาน รับรองว่ามวลจะเพิ่มขึ้น 18:1 การใช้ทรัพยากรในท้องถิ่นนี้จะส่งผลให้ประหยัดน้ำหนักและต้นทุนได้อย่างมากในภารกิจที่มีคนขับไปยังดาวอังคาร (หรือภารกิจส่งดินอัตโนมัติ)
มูลนิธิวิกิมีเดีย 2010.
ดูว่า "ปฏิกิริยา Sabatier" ในพจนานุกรมอื่น ๆ คืออะไร:
Wikipedia มีบทความเกี่ยวกับบุคคลที่มีนามสกุลนี้ ดูที่ Sabatier พอล ซาบาเทียร์ พอล ซาบาเทียร์ ... Wikipedia
Paul Sabatier Paul Sabatier (ฝรั่งเศส Paul Sabatier) (5 พฤศจิกายน พ.ศ. 2397, Carcassonne - 14 สิงหาคม พ.ศ. 2484 ตูลูส) นักเคมีชาวฝรั่งเศสผู้ได้รับรางวัลโนเบลสาขาเคมีประจำปี พ.ศ. 2455 ชีวประวัติ เกิดในครอบครัวของนักธุรกิจ Alexis Sabatier; มัธยมศึกษา ... วิกิพีเดีย
- (ฝรั่งเศส Paul Sabatier) (5 พฤศจิกายน พ.ศ. 2397 การ์กาซอน - 14 สิงหาคม พ.ศ. 2484 ตูลูส) นักเคมีชาวฝรั่งเศสผู้ได้รับรางวัลโนเบลสาขาเคมีประจำปี พ.ศ. 2455 ชีวประวัติ เกิดในครอบครัวของนักธุรกิจ Alexis Sabatier; มัธยมศึกษา ... วิกิพีเดีย
- (สารเคมี) ชื่อเดิมที่ตั้งให้กับไฮโดรคาร์บอนที่ได้จากการไฮโดรจิเนชันของเบนซีนและสารที่คล้ายคลึงกันบางส่วน (Berthelot, Bayer, Vreden) เนื่องจากสารเหล่านี้ได้รับการพิจารณา (ตามองค์ประกอบของสารเหล่านั้น) ว่าเป็นผลิตภัณฑ์ที่มีการรวมกันโดยตรง... ... พจนานุกรมสารานุกรม F.A. บร็อคเฮาส์ และ ไอ.เอ. เอฟรอน
ข้อมูลในบทความนี้หรือบางส่วนล้าสมัย คุณสามารถช่วยโครงการได้... Wikipedia
- (ฝรั่งเศส) สาธารณรัฐฝรั่งเศส (République Française) I. ข้อมูลทั่วไป F. รัฐในยุโรปตะวันตก ทางตอนเหนือ อาณาเขตของฝรั่งเศสถูกล้างด้วยทะเลเหนือ ปาสเดอกาเลส์ และช่องแคบช่องแคบอังกฤษ ทางตะวันตกคืออ่าวบิสเคย์... ... สารานุกรมผู้ยิ่งใหญ่แห่งสหภาพโซเวียต
และ ใบเสร็จ
1. ปฏิกิริยาเวิร์ทซ
: ผลของโซเดียมโลหะต่อไฮโดรคาร์บอนโมโนฮาโลเจน โครงกระดูกคาร์บอนเพิ่มขึ้นเป็นสองเท่า ปฏิกิริยานี้เหมาะสำหรับการเตรียมอัลเคนแบบสมมาตร
2CH 3 –CH 2 ห้องนอน + 2Na = CH 3 –CH 2 –CH 2 –CH 3 +2NaBr
2. ปฏิกิริยา ดูมาส์: ดีคาร์บอกซิเลชันของเกลือของกรดคาร์บอกซิลิก - ฟิวชั่นกับด่าง
CH 3 COONa (ทีวี) + NaOH (ทีวี) = CH 4 + Na 2 CO 3
3. ปฏิกิริยา โคลเบ: อิเล็กโทรไลซิสของสารละลายเกลือของกรดคาร์บอกซิลิก:
CH 3 COONa + 2H 2 O = [กระแสไฟฟ้า] = 2CO 2 + H 2 + C 2 H 6 + 2NaOH
4. การสังเคราะห์ กุสตาฟสัน: กำจัดอะตอมฮาโลเจนสองอะตอมออกจากไดฮาโลอัลเคน:
ClCH2-CH2-CH2-CH2Cl + Zn = C 4 H 8 (ไซโคลบิวเทน) + ZnCl 2
สามารถใช้สังกะสีแทนแมกนีเซียมได้
5. การสังเคราะห์ เลเบเดวา: ได้บิวทาไดอีนจากเอธานอล
2C2H5OH = ชม. 2 + 2H 2 O + CH2=CH-CH=CH2
คุณสมบัติทางเคมี
1. ปฏิกิริยา โคโนวาโลวา– ไนเตรตของอัลเคนด้วยกรดไนตริกเจือจาง (10%):
C 2 H 6 + HNO 3 = C 2 H 5 NO 2 + H 2 O
หัวกะทิของไนเตรต:
อะตอมระดับตติยภูมิ อะตอมรอง อะตอมคาร์บอนปฐมภูมิ
2. ผลกระทบ
ฮาราชา:การเติมไฮโดรเจนโบรไมด์เมื่อมีเปอร์ออกไซด์ ปฏิกิริยาดังกล่าวขัดต่อกฎของ Markovnikov:
CH 3 -CH = CH 2 + HBr = [H 2 O 2 ] = CH 3 -CH 2 -CH 2 Br
3. ปฏิกิริยา วากเนอร์: ทำปฏิกิริยากับสารละลายน้ำเย็นของโพแทสเซียมเปอร์แมงกาเนต - ออกซิเดชันเล็กน้อยของอัลคีน (เกิดไดออล)
3CH 3 -CH = CH 2 + 2KMnO 4 + 4H 2 O = 2MnO 2 + 2KOH + 3CH 3 -CH (OH) -CH 2 (OH)
4. ปฏิกิริยา คูเชโรวา: ความชุ่มชื้นของอัลคีน การเติมน้ำเกิดขึ้นเมื่อมีเกลือของปรอท (II) และเกิดขึ้นผ่านการก่อตัวของอีนอลที่ไม่เสถียร ซึ่งไอโซเมอร์ไรซ์เป็นอัลดีไฮด์หรือคีโตน การให้น้ำของอะเซทิลีนทำให้เกิดอัลดีไฮด์ และอัลคีนอื่นๆ จะให้คีโตน
C 2 H 2 + H 2 O = CH 3 C H O
5. ปฏิกิริยา เซลินสกี้: ไตรเมอร์ไรเซชันของอะเซทิลีนเหนือถ่านกัมมันต์ เบนซินจะเกิดขึ้น
3C 2 ชั่วโมง 2 = ค 6 ชั่วโมง 6
6. ปฏิกิริยา ซินิน่า: การลดลงของสารประกอบไนโตรในสารละลายในสภาพแวดล้อมที่เป็นด่างและเป็นกลาง:
R-NO 2 + 3(NH 4) 2 S = R-NH 2 + 3S + 6NH 3 +2H 2 O
สิ่งที่รวมเราเป็นหนึ่งเดียว...
ปฏิกิริยา Arbuzov (การจัดเรียง Arbuzov ใหม่, Arbuzov isomerization)ตัวเร่งปฏิกิริยาไอโซเมอไรเซชันของเอสเทอร์ของกรดฟอสฟอรัสเป็นเอสเทอร์ของกรดอัลคิลฟอสฟินิก (1904)
กฎของไบล์สไตน์หากองค์ประกอบทดแทนทั้งสองบนวงแหวนอะโรมาติกเป็นประเภทเดียวกัน ทิศทางที่โดดเด่นของการทดแทนจะถูกกำหนดโดยผู้ที่มีอิทธิพลมากกว่า (1866)
การทดสอบไบล์สไตน์การค้นพบฮาโลเจนในสารประกอบอินทรีย์โดยการเผาบนลวดทองแดงออกซิไดซ์ ( 1872 ). สารที่ผสมกับ CuO จะถูกนำไปใช้กับลวดทองแดง (หรือแพลตตินัม) และนำเข้าไปในเปลวไฟ คอปเปอร์เฮไลด์ที่ระเหยได้จะทำให้เปลวไฟเป็นสีเขียวหรือเขียวอมฟ้า
รีเอเจนต์เบเนดิกต้า (พยายามเบเนดิกต้า) . การตรวจหาอะลิฟาติกอัลดีไฮด์โดยการกระทำของสารละลายในน้ำที่ประกอบด้วยคอปเปอร์(II) ซัลเฟต CuSO 4, โซเดียมคาร์บอเนต Na 2 CO 3 และโซเดียมซิเตรต เมื่อได้รับความร้อน จะเกิดตะกอนสีแดง เหลือง และเขียว
ปฏิกิริยาโบโรดินการสลายตัวของยูเรีย:
ปฏิกิริยาของบัตเลรอฟ-เลอร์มอนโตวา-เอลเทคอฟการเตรียมไฮโดรคาร์บอนของโครงสร้างไอโซซิสโดยการเร่งปฏิกิริยาอัลคิเลชันของโอเลฟินส์ตอนล่างด้วยอัลคิลเฮไลด์ (1878)
ปฏิกิริยาของวากเนอร์ (ออกซิเดชันของวากเนอร์, การทดสอบเปอร์แมงกาเนต)ออกซิเดชันของสารประกอบอินทรีย์ที่มีพันธะคู่โดยการกระทำของสารละลายโพแทสเซียมเปอร์แมงกาเนต 1-3% ( 1887 ) วี ถูกต้อง-a-glycols ในสภาพแวดล้อมที่เป็นด่าง (ถือว่าเป็นบวกหากสารละลายเปอร์แมงกาเนตเปลี่ยนสีอย่างรวดเร็วในสภาพแวดล้อมที่เป็นกรดหรือเปลี่ยนเป็นสีน้ำตาลในสภาพแวดล้อมที่เป็นด่างและเป็นกลาง):
ปฏิกิริยาของเวอเลอร์ปฏิกิริยาระหว่างแคลเซียมคาร์ไบด์กับน้ำ (2405) ปฏิกิริยาดังกล่าวมีความสำคัญในทางปฏิบัติหลังจากที่ A. Moissan และ T. Wilson พัฒนาวิธีการผลิตแคลเซียมคาร์ไบด์ในเตาไฟฟ้าในราคาถูกโดยการหลอมโค้กและมะนาว (1892)
ปฏิกิริยาวิลเลียมสัน (วิธีวิลเลียมสัน). การเตรียมอีเทอร์จากอัลคิลเฮไลด์และโซเดียม (หรือโพแทสเซียม) อัลคอกไซด์: 
ปฏิกิริยาเวิร์ทซ. . การสังเคราะห์อัลเคนโดยการกระทำของโซเดียมโลหะในตัวทำละลายเฉื่อยบนอัลคิลเฮไลด์ (1855):
โดยทั่วไป:
ปฏิกิริยา Wurtz-Fittig . การเตรียมอัลคิลเบนซีนจากส่วนผสมของอะลิฟาติกและอะโรมาติกเฮไลด์โดยการกระทำของโซเดียมโลหะในตัวทำละลายเฉื่อย (2407):
ปฏิกิริยาของแฮรี่ส์(พ.ศ. 2409-2466) ศาสตราจารย์ (เยอรมนี) งานวิจัยหลักเกี่ยวกับเคมีของยาง ประธานสมาคมเคมีแห่งเยอรมัน (พ.ศ. 2463-2465) การก่อตัวของโอโซน
ปฏิกิริยาของกัตเตอร์แมนการเตรียมอะโรมาติกอัลดีไฮด์โดยปฏิกิริยาของฟีนอลกับไฮโดรเจนคลอไรด์และไฮโดรเจนไซยาไนด์ต่อหน้าตัวเร่งปฏิกิริยา (กรดลูอิส) ตามด้วยการไฮโดรไลซิสของผลิตภัณฑ์ (2441): 
กฎการวางแนวของฮอลเลอมันน์ทิศทาง (องค์ประกอบทดแทน) ประเภทแรก (CH 3 , C 2 H 5 , ฮาโลเจน, หมู่อะมิโน, ไฮดรอกซิล) เพิ่มปฏิกิริยาของวงแหวนอะโรมาติกและควบคุมรีเอเจนต์ไปยังตำแหน่งออร์โธและพารา
2. การวางแนว (องค์ประกอบย่อย) ประเภทที่สอง (หมู่ไนโตรและซัลโฟ, หมู่คาร์บอกซิลและคาร์บอนิล) ลดปฏิกิริยาของวงแหวนอะโรมาติกและกำหนดทิศทางรีเอเจนต์ไปยังตำแหน่งเมตาดาต้า (1895) (ขณะนี้มีการอธิบายผลกระทบเหล่านี้ตามแนวคิดทางอิเล็กทรอนิกส์: ผลกระทบแบบมีโซเมอร์และอุปนัย, 1920)
ปฏิกิริยาของฮอฟฟ์แมนน์. การเตรียมอะลิฟาติกเอมีนจากอัลคิลเฮไลด์: 
และต่อๆ ไปจนเกิดเป็นเอมีนตติยภูมิ (CH 3) 3 N.
รีเอเจนต์กริกนาร์ด. การสังเคราะห์สารอินทรีย์จากอัลคิลเฮไลด์และแมกนีเซียมในอีเทอร์ ปฏิกิริยานี้ถูกค้นพบโดย P. Barbier ในปี พ.ศ. 2442 และศึกษาโดยละเอียดโดย V. Grignard ในปี พ.ศ. 2443:
รีเอเจนต์กรินาร์ด RMgX ใช้สำหรับการเติมในพันธะหลายพันธะ 
ปฏิกิริยาของกุสตาฟสัน. การเตรียมไซโคลอัลเคนจากอนุพันธ์ของไดฮาโลเจน ( 1887
). 
ปฏิกิริยาไดลส์-ออลเดอร์ (การสังเคราะห์ไดอีน ) การเติมสารประกอบไม่อิ่มตัวซึ่งมีพันธะหลายตัวถูกกระตุ้นโดยกลุ่มใกล้เคียง (สารประกอบดังกล่าวเรียกว่า " ไดโนฟิล": อะโครลีน, มาโลนิกแอนไฮไดรด์, โครโตนัลดีไฮด์) ให้เป็นไฮโดรคาร์บอนไม่อิ่มตัว ( ตาย) ซึ่งมีพันธะคู่แบบคอนจูเกต (บิวทาไดอีน, ไซโคลเฮกซาไดอีน, แอนทราซีน, ฟูแรน) (1928)
กฎของ Zaitsev. การกำจัดกรดไฮโดรฮาลิกจากอัลคิลเฮไลด์หรือน้ำจากแอลกอฮอล์ส่วนใหญ่เกิดขึ้นในลักษณะที่ไฮโดรเจนจากอะตอมคาร์บอนที่อยู่ใกล้เคียงที่ถูกเติมไฮโดรเจนน้อยที่สุดออกไปพร้อมกับฮาโลเจนหรือไฮดรอกซิล ( 1875
): 
ปฏิกิริยา Zelinsky-Kazansky (วิธี Zelinsky-Kazansky). ไตรเมอไรเซชันของอะเซทิลีน (พอลิเมอไรเซชันของอะเซทิลีน) บนถ่านกัมมันต์เมื่อถูกความร้อน (1924)
: 
ปฏิกิริยาเซลินสกี้ (ตัวเร่งปฏิกิริยาที่ไม่สามารถย้อนกลับได้, ตัวเร่งปฏิกิริยาเซลินสกี้)สัดส่วนตัวเร่งปฏิกิริยาของไซโคลเฮกซาไดอีนและไซโคลเฮกซีน (1911): 
ปฏิกิริยาของซินิน. การลดสารประกอบอะโรมาติกไนโตร ( 1842
): ![]()
ปฏิกิริยาของคันนิซซาโร. สัดส่วนรีดอกซ์ของอัลดีไฮด์อะโรมาติกสองโมเลกุลในตัวกลางที่เป็นด่างซึ่งนำไปสู่การก่อตัวของแอลกอฮอล์และกรด (1853): 
ปฏิกิริยาของเคอร์ชอฟฟ์. การเตรียมกลูโคสโดยการไฮโดรไลซิสของแป้งโดยให้ความร้อนด้วยตัวเร่งปฏิกิริยา - กรดซัลฟิวริกเจือจาง ( 1811 ):
ปฏิกิริยาเคลมเมนเซน (การลดเคลมเมนเซน). การลดอัลดีไฮด์และคีโตนให้กลายเป็นความคล้ายคลึงของเบนซีนด้วยไฮโดรเจน ณ เวลาที่แยกออก (การลดกลุ่มคาร์บอนิลเป็นเมทิลีน) (1913):
ปฏิกิริยาโคลเบ-ชมิทท์. การเตรียมกรดอะโรมาติกไฮดรอกซีโดยคาร์บอกซิเลชั่นของฟีโนเลตโลหะอัลคาไล (1860): 
ปฏิกิริยาโคลเบ (เคมีไฟฟ้า). การเตรียมอัลเคนที่มีอะตอมคาร์บอนจำนวนคู่โดยอิเล็กโทรไลซิสของสารละลายเกลือโลหะอัลคาไลและกรดคาร์บอกซิลิกด้วยสายโซ่คาร์บอนตรง (1849):
ปฏิกิริยาของโคโนวาลอฟ. การเตรียมไนโตรอัลเคน ( 1888 ):
ปฏิกิริยา Kucherov (การให้ความชุ่มชื้นของ Kucherov). การเร่งปฏิกิริยาไฮเดรชั่นของอะเซทิลีนไฮโดรคาร์บอนด้วยการก่อตัวของสารประกอบที่ประกอบด้วยคาร์บอนิล ( 1881
):
ปฏิกิริยาของเลเบเดฟ. การเตรียมบิวทาไดอีนโดยไพโรไลซิสของเอธานอล (1926 ):
ปฏิกิริยาของ Lvov-Sheshukov. การคลอรีนของโอเลฟินส์ไปยังตำแหน่ง a ของพันธะคู่ พร้อมด้วยการเปลี่ยนแปลงของอัลลิลิกของพันธะคู่ (1883):
กฎของมาร์คอฟนิคอฟ. ในกรณีของการเติมสารประกอบที่มีไฮโดรเจน (กรดโปรติกหรือน้ำ) ให้กับอัลคีนที่ไม่สมมาตร อะตอมของไฮโดรเจนจะเกาะติดกับอะตอมของคาร์บอนที่เติมไฮโดรเจนมากที่สุดซึ่งอยู่ที่พันธะคู่ ( 1869 ):
ปฏิกิริยา Nastyukov (ปฏิกิริยาฟอร์มาไลต์). ปฏิกิริยาของอะโรมาติกไฮโดรคาร์บอนกับฟอร์มาลดีไฮด์ (การกำหนดอะโรมาติกไฮโดรคาร์บอน) ต่อหน้ากรดซัลฟิวริกเข้มข้น (1904):
การก่อตัวของเรซินสีน้ำตาลแดงเป็นการยืนยันการมีอยู่ของเบนซีนและความคล้ายคลึงกัน ปฏิกิริยาถูกขัดขวางโดยการมีอยู่ของสารประกอบไซคลิกไม่อิ่มตัว
กฎของเนสเมยานอฟ-โบริซอฟ. การแทนที่ด้วยไฟฟ้าและอนุมูลอิสระที่อะตอมของคาร์บอนที่เชื่อมต่อกันด้วยพันธะคู่ของคาร์บอน-คาร์บอนเกิดขึ้นในขณะที่ยังคงรักษาโครงสร้างทางเรขาคณิตของโมเลกุลของสารไว้
ปฏิกิริยาไรเมอร์-ไทมันน์. การได้รับอะโรมาติก โอ-ออกซีอัลดีไฮด์โดยทำปฏิกิริยาฟีนอลกับคลอโรฟอร์มในสารละลายด่าง ปฏิกิริยาแนะนำหมู่อัลดีไฮด์เข้าไปในวงแหวนเบนซีน (การแทนที่มักเกิดขึ้นที่ตำแหน่งออร์โธ):
ปฏิกิริยาของโรเซนมันด์. การเตรียมอะโรมาติกอัลดีไฮด์จากกรดคลอไรด์ในสภาพแวดล้อมของเบนซีน โทลูอีน และอะโรมาติกไฮโดรคาร์บอนอื่นๆ:
ปฏิกิริยานี้ถูกค้นพบโดย M.M. Zaitsev ในปี พ.ศ. 2415 และศึกษารายละเอียดโดย K.V. Rosenmund ในปี พ.ศ. 2461
ปฏิกิริยาซาบาติเยร์-ซุนเดอรัน. การเติมไฮโดรเจนในเฟสของเหลวของเอทิลีนเป็นอีเทนโดยมีนิกเกิลแบ่งละเอียดเป็นตัวเร่งปฏิกิริยา (1899):
ปฏิกิริยาของ Savich. การเตรียมอัลไคน์จากอนุพันธ์ไดฮาโลเจนของอัลเคน (1861):
การทดสอบของเซลิวานอฟ. การค้นพบเชิงคุณภาพฟรุกโตส ( 1887
) (คีโตสเมื่อถูกความร้อนด้วยเรซอร์ซินอลและกรดไฮโดรคลอริกจะให้สีแดงเชอร์รี่ อัลโดสภายใต้สภาวะเดียวกันจะทำปฏิกิริยาช้ากว่าและให้สีชมพูอ่อน):
(คุณสามารถใช้สารละลายที่ประกอบด้วยรีซอร์ซินอล 0.05 กรัมในน้ำ 50 มิลลิลิตร และกรดไฮโดรคลอริกเข้มข้น 2-3 หยดที่มีความหนาแน่น 1.19 กรัม/มิลลิลิตร)
ปฏิกิริยาของทิชเชนโก้. สัดส่วนของอัลดีไฮด์ - การได้รับเอสเทอร์จากอัลดีไฮด์ - เมื่อมีอะลูมิเนียมอัลคอกไซด์ (1906):
การทดสอบโทลเลน (ปฏิกิริยา "กระจกสีเงิน"). ปฏิกิริยาของฟอร์มาลดีไฮด์กับสารละลายแอมโมเนียของซิลเวอร์ออกไซด์ (สารทำปฏิกิริยา Tollens):
ปฏิกิริยาของอุลมานน์. การเตรียมความคล้ายคลึงกันของอะโรมาติกที่สูงขึ้นจากอาริลเฮไลด์โดยการกระทำของทองแดงที่เป็นผง:
ปฏิกิริยาของฟาวสกี้. การควบแน่นของสารประกอบคาร์บอนิลกับอัลคีนเพื่อสร้างอะเซทิลีนแอลกอฮอล์:
การสังเคราะห์ฟิสเชอร์-ทรอปส์. การเตรียมอัลเคนโดยตัวเร่งปฏิกิริยาไฮโดรจิเนชัน (ปฏิกิริยากับไฮโดรเจน) ของคาร์บอนมอนอกไซด์ภายใต้ความดัน (1923)
ปฏิกิริยาโฟไคน์. การเติมไฮโดรเจนของไขมัน (1902):
ปฏิกิริยาของฟรีเดล-คราฟต์. อัลคิเลชันหรืออะซิเลชันของสารประกอบอะโรมาติกตามลำดับด้วยอัลคิลหรือเอซิลเฮไลด์ (การเตรียมเบนซีนที่คล้ายคลึงกัน) ต่อหน้าตัวเร่งปฏิกิริยาปราศจากน้ำ (AlCl 3, BF 3, ZnCl 2 ฯลฯ ) (1877):
ปฏิกิริยา Chugaev (ปฏิกิริยาแซนโทเจน). การเปลี่ยนแอลกอฮอล์เป็นอัลคีนโดยการสลายตัวด้วยความร้อนของแซนโทเจนอีเทอร์ที่ได้จากแอลกอฮอล์เหล่านี้ (1902)
แคร็กตาม Shukhov. การแปรรูปวัตถุดิบตั้งต้นปิโตรเลียมที่อุณหภูมิสูงเพื่อให้ได้ผลิตภัณฑ์ที่มีน้ำหนักโมเลกุลต่ำกว่า - การแยกไฮโดรคาร์บอนปิโตรเลียม (2434)
กฎของ Eltekov (การจัดเรียงใหม่ของ Eltekov). สารประกอบที่หมู่ไฮดรอกซิลตั้งอยู่ที่อะตอมของคาร์บอนซึ่งก่อให้เกิดพันธะหลายคาร์บอน - คาร์บอน (อีนอล) จะไม่เสถียรและไอโซเมอร์ไรซ์เป็นสารประกอบคาร์บอนิลที่สอดคล้องกัน - อัลดีไฮด์หรือคีโตน (1877):
ปฏิกิริยาของยูริเยฟ. อินเตอร์คอนเวอร์ชันของสารประกอบเฮเทอโรไซคลิก 5 สมาชิกที่มีหนึ่งเฮเทอโรอะตอม (1936)